流式细胞术系统和方法与流程
本发明通常涉及生物技术,以及更具体地涉及流式细胞术。
背景技术:
流式细胞术是流体流动系统组织流体流内的细胞使得细胞以单列通过检测区的技术。当细胞通过检测区时,细胞被激光照射,激光以取决于细胞结构的方式从每个细胞散射。大多数现代流式细胞术方法还采用与特定细胞特征选择性地结合的许多荧光染料标记的抗体,诸如细胞相关分子、蛋白质或者配体。当在它们的相应激发波长下受到光激发时,每个荧光染料发射特征荧光信号,指示该特异于荧光染料的特征的存在。对所散射的光和荧光信号进行检测和分析以根据一组感兴趣的参数对细胞进行分类和/或计数。在一些情况下,一旦被分类,细胞就基于它们的特定特征分成亚群。
流式细胞术使能流体流中单个细胞的同时多参数分析(诸如分析细胞表面和细胞内分子)、混合细胞群体中的不同细胞类型的表征和定义、评估分离亚群的纯度以及分析细胞大小和体积。流式细胞仪用于许多临床和生物应用,诸如血癌的诊断、基础研究、临床实践和临床试验。
在历史上,常规流式细胞仪中的流体流动系统具有空气流构造,在该空气流构造中,流体流被迫通过喷嘴系统,使得细胞以单列通过开放空间中的检测区。其它现有技术流式细胞仪采用流动单元构造,其中鞘流体以流体动力学的方式将样本流体聚焦到穿过检测区的开放流的核心中。可惜,在每个情况下,这种现有技术流式细胞仪都具有一些显著缺点:(1)它们非常昂贵;(2)它们具有大占用面积;(3)它们不易于携带;以及(4)它们需要大量时间、专业技术和开销来使用和维护。另外,具有开放流动设计的系统由于暴露风险很难适用于传染性疾病或者病原性微生物样本。
为了缓和这些中的一些缺点,开发了样本流体穿过封闭流动通道中的检测区的基于微流体的流式细胞仪。采用微流体方法还使能提高的芯片上功能,诸如过滤、细胞分类和总体流动控制。
例如在美国专利公开No.2009/0051912中公开了基于微流体的流式细胞仪,该美国专利公开描述了比开放流动系统更小并且更便携的流式细胞仪系统。在操作中,将流体流动系统固定在显微镜物镜下,该显微镜物镜起到提供用于询问细胞的光以及收集从检测区散射或者发出的光的外部光学系统的作用。
事实上,大多数常规流式细胞仪依靠外部光学器件照射检测区和/或检测散射的光信号。可惜,这限定了流式细胞仪可以被制造得多小以及多便携。另外,流体流动系统与外部光学器件之间的精细对准是实现精确和准确测量的关健,以及必须在使用期间保持该对准以确保正确的系统操作。若干荧光染料的使用通常引起对不同激发波长下的多个激光器的需要,用以激发所采用的一托盘荧光染料,进一步加剧了这些问题。更进一步地,需要许多过滤波长检测器以有效地区分合成荧光信号。因此,使用外部光学器件会使流式细胞术系统增加显著的成本。
使光学表面波导与微流体流体流动系统集成在一起为缓和基于外部光学器件的流式细胞仪的缺点中的一些提供了一定的希望。在美国专利No.7,764,374中公开了具有集成的光学表面波导的基于微流体的系统的示例,在该示例中,在衬底顶表面上形成流体流动通道和基于SU-8的光学表面波导两者。一个SU-8表面波导将光发射到流体流动通道的分析区中,而跨越流体流动通道设置的第二SU-8表面波导在光穿过分析区之后收集光。
以类似的方式,美国专利公开No.2013/0083315公开了具有包括检测区的第一流动通道以及邻近检测区的多个“表面波导通道”的流式细胞仪布置。表面波导通道充满将从检测区捕获的光侧向地引导至衬底其它区域的流体。
可惜,这种现有技术系统遭受若干缺点。通常需要使若干独立光信号耦合到单个区域中或者从单个区域耦合出。然而,基于SU-8的表面波导和充满流体的表面波导需要很大的芯片有效面积。因此,形成超过几个接入相同位置的光学表面波导是具有挑战性的。
此外,当用基本上均匀的光照射检测区时,流式细胞术性能提高。然而,现有技术基于微流体的流式细胞仪限于提供从流体通道的一侧进行的照射。因此,使得样本流体的均匀照射不可能以及系统灵敏度降低。
技术实现要素:
本发明使能改进了流体流的照射和/或改进了由流体流产生的光信号的检测的芯片上实验室系统。因此,本发明的实施例能够提供比现有技术芯片上实验室系统更好的系统性能、更小的测量变化以及更高的灵敏度。例如,根据本发明的基于芯片上实验室流式细胞仪可以以提高的精确度区分不同的细胞亚群以及可以比现有技术中已知的流式细胞仪更好地量化测量参数。尽管本发明特别地适合在流式细胞仪中使用,但是它还在其它芯片上实验室系统(诸如,频谱仪等等)中提供优点。
本发明的例示性实施例是具有穿过衬底厚度形成的流体通道以及设置在衬底表面上的两组表面波导的流式细胞术系统。每组表面波导被布置为使得其端面围绕流动通道形成圆形布置。在与穿过通道的流体流动方向基本上正交的不同平面中形成每组表面波导。
第一组表面波导用于照射检测区。来自这些激发波导的光在流动通道中形成基本上均匀的照射图案。在一些实施例中,控制激发波导中的一个或者多个中的光的相位,从而使能对检测区中的照射图案的形状的控制。
第二组表面波导用于在光与检测区中的流体相互作用之后捕获光。在一些实施例中,这些收集波导中的一个或者多个中的光的相位是可控制的。在一些实施例中,收集波导中的至少一个与波长滤波器光学地耦合,该波长滤波器辨别耦合到该收集波导中的光中的光谱信息。
在一些实施例中,至少一组表面波导被布置为使得它们的小面围绕流动通道形成多边形布置。在这些实施例中的一些中,多边形的每个边包括多个表面波导小面。
本发明的实施例是这样一种装置,包括:衬底,限定第一平面,衬底包括流动通道,可操作用于沿着与第一平面基本上正交的第一方向输送流体,流动通道位于衬底的第一区域内;第一表面波导,与流动通道光学地耦合,第一表面波导位于第一区域内的第二平面中,其中第二平面与第一平面基本上平行;以及第二表面波导,与第一区域中的流动通道光学地耦合,第二表面波导位于第一区域内的第三平面中,其中第三平面与第二平面基本上平行。
本发明的另一个实施例是这样一种装置,包括:衬底,具有第一主表面与第二主表面之间的厚度;第一流动通道,可操作用于穿过厚度输送流体;多个第一表面波导,多个第一表面波导中的每一个与第一区域中的流动通道光学地耦合,多个第一表面波导在第一区域内的第一平面中共面;以及多个第二表面波导,多个第二表面波导中的每一个与流动通道光学地耦合,多个第二表面波导在第一区域内的第二平面中共面;其中,第一主表面、第二主表面、第一平面与第二平面基本上平行。
本发明的又另一个实施例是这样一种方法,包括:沿着第一方向输送第一流体穿过第一区域;用第一照射图案询问第一流体,所述第一照射图案基于从位于与第一区域中的第一方向正交的第一平面中的第一表面波导发出的第一光信号;以及使第一照射图案的第一部分耦合到位于与第一区域中的第一方向正交的第二平面中的第二表面波导中,其中在第一照射图案与第一流体相互作用之后,第一部分耦合到第二表面波导中。
附图说明
图1A-C描绘了具有集成表面波导的现有技术微流体系统的示例。
图2描绘了根据本发明例示性实施例的流式细胞仪的框图。
图3描绘了根据例示性实施例用于执行流式细胞术的方法的操作。
图4描绘了根据本发明例示性实施例的光流体系统的横截面视图的示意图。
图5描绘了用于形成光流体系统204的方法的操作。
图6描绘了光学板404的俯视图。
图7A-B描绘了光学板404的区域602的俯视图和横截面视图。
图8描绘了适用于形成光学板404的子操作。
图9A描绘了在限定波导芯706之后区域602的俯视图的示意图。
图9B描绘了在限定波导芯714之后区域602的俯视图的示意图。
图10描绘了询问细胞226期间的检测区414的侧视图。
图11描绘了根据本发明第一替换实施例的区域602的俯视图的示意图。
图12A-C描绘了对于不同波长的光的整个检测区1106上的模拟照射图案。
图13A-C描绘了对于不同波长的激发光的整个检测区1106上的随机相位场分布的曲线图。
图14描绘了根据本发明第二替换实施例的光学板。
图15A和和15B分别地描绘了根据本发明第二替换实施例的相位控制元件1402-E-i和1402-C-i的横截面视图。
图16描绘了激发波导芯706-i根据压电层1506的厚度、长度和宽度的有效折射率的变化的模拟结果。
图17描绘了根据现有技术的常规流式细胞仪流动单元的图片。
图18A-B描绘了根据本发明第三替换实施例的流式细胞术流动单元。
具体实施方式
图1A-C描绘了具有集成表面波导的现有技术微流体系统的示例。
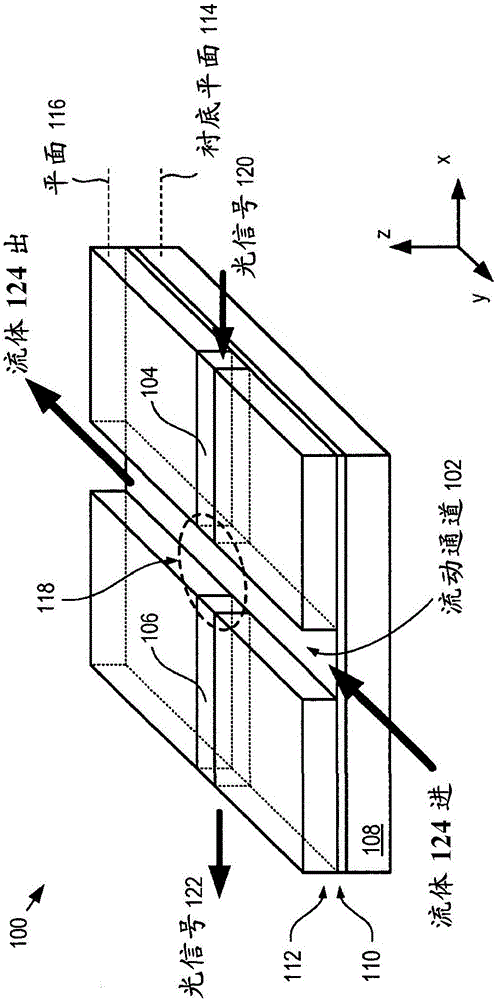
图1A描绘了微全分析系统(μTAS)的一部分,包括流动通道102、照射波导104和收集波导106,在衬底108的顶表面上形成这些中的全部。系统100根据J.Hubner等人在2010年7月27日授权的美国专利No.7,764,374中公开的芯片上实验室(LOC)系统,该美国专利通过引用合并于此。
系统100是吸收光谱系统的示例。在操作中,照射波导104将光信号120发射到分析区118中,该分析区118由照射波导104与收集波导106之间的区域限定。流体124基于流体的成分吸收特定特征波长的光。没有被流体吸收的光中的一些被收集波导106捕获为光信号122,该光信号122将光传送至使能其光谱分析的波长色散系统(未示出)。
在衬底108的顶表面上形成照射波导104和收集波导106以及流动通道102。衬底108典型地包括硅,在该衬底108上二氧化硅层(即,下包覆110)形成为波导的下包覆层。衬底108限定与x-y平面对准的衬底平面114。
波导中的每一个包括由层112包围的SU-8的芯区,该芯区作用以横向地限定波导中的光信号120和122。层112典型地为设置在下包覆层110上的二氧化硅层。应当注意,层112限定平行于衬底平面114的平面116。流动通道102以及波导104和106都在平面116中共面。
为了完成波导结构以及封闭流动通道102,将具有第三二氧化硅层的第二衬底(为了清晰起见,未示出)键合至层112。
尽管缓和了上面讨论的与基于微流体的分析系统相关的缺陷中的一些,但是系统100仍然具有一些显著缺陷。例如,通过形成所有表面波导和流动通道以使得它们共面,对分析区118的光学接入主要限于仅一个表面波导对。因此,使得由沿不同路径传播的超过一个光信号同时询问分析区不可能。因此,为了用多个光信号询问流体110,需要多对照射和收集波导,这导致系统100的增大的芯片有效面积以及相对应的更高成本。此外,在需要收集由分析区118中的材料散射的光的应用中,仅可以通过收集波导收集前向散射光。在位置处形成以捕获侧面散射光的表面波导通常将分隔相对较大的距离,使得表面波导很难捕获足够的光用于可靠测量。此外,由于光吸收,在系统100中使用SU-8可以随时间导致降解(特别地当系统用于短波长和/或高强度时)。
图1B-C分别地描绘了具有集成微流体和表面波导的芯片上实验室系统的另一个示例的俯视图和横截面视图的示意图。系统126是部分集成的流式细胞仪的一部分的示例。系统126包括流动通道128、表面波导130-1至130-N和激光器132-1至132-N。系统126根据C.Vannahme等人在Optics Express(Vol.19,No.9,pp.8179-8186(2011))的“Plastic lab-on-a-chip for fluorescence excitation with integrated organic semiconductor lasers”中描述的流式细胞仪,该内容通过引用合并于此。
系统126包括流动通道128、表面波导130和激光器132,这些中的全部单片地集成在衬底138上。如上面描述的系统100,所有流动通道和表面波导在衬底平面150中共面。
衬底138是使用常规塑料压印技术使流动通道128和凹陷部分140在其中形成的聚(甲基丙烯酸甲酯)(PMMA)衬底。形成凹陷部分140以使得每个凹陷部分的底部由初生光栅结构142表征,稍后用有机半导体三(8-羟基喹啉)铝(Alq3)薄膜涂敷该初生光栅结构142以形成有机半导体激光器132。
通过将PMMA材料暴露于深UV光以在PMMA材料中直接地形成表面波导130,该深UV光使PMMA材料中的分子链断裂以局部地增大其折射率。未暴露的PMMA保持其最初的较低折射率,使其能够充当波导的包覆材料。
在限定表面波导之后,PMMA盖144接合至衬底138以完成系统126的制造。
在操作中,激光器132被光学地泵浦以生成光信号146-1至146-N,分别地耦合到表面波导130-1至130-N中。光信号146用于激发用于将流体136中的分析物染色的不同荧光染料。随着流体中的细胞顺序地流过检测区134-1至134-N中的每一个,与细胞特征选择性结合的荧光染料以它们的特征荧光波长发荧光为光信号148-1至148-N。
荧光信号148从平面150传播出去以及通过基于自由空间光学器件的检测系统进行检测。
提供不同检测区以使得可以使用多个激发信号激发整个托盘的荧光染料的需要对系统126及其工作增加了显著的复杂度。例如,由于并非同时激发荧光染料,因此模糊度会影响测量结果。此外,对外部自由空间检测系统的需要减少了集成流动通道128与表面波导130的益处中的许多。更进一步地,如上面讨论的,多个检测区需要更大的芯片有效面积,这导致更高的系统成本。
本发明通过将多个表面波导布置在不与流动通道输送流体的方向共面的平面中以使能改进的流式细胞术。因此,可以将表面波导的小面布置在流动通道的不同侧上。因此,本发明通过照射流体的方式使能更好的控制。即使光沿着不同方向离开流动通道,也通过使能靠近流动通道收集光以提高从流动通道收集光的能力。
应当注意,尽管本发明特别地适合于流式细胞术,但是还可以在其它微流体应用(诸如,光谱学、化学合成、毛细管电泳、芯片上实验室应用等等)中提供类似的优点。
图2描绘了根据本发明例示性实施例的流式细胞仪的框图。流式细胞仪200包括光源202、光流体系统204、检测器206和处理器208。
系统200可操作用于分析液相流体224中包括的细胞226。在一些实施例中,系统200可操作用于液相介质中包括的其它颗粒。在一些实施例中,系统200可操作用于气相介质(例如,空气等等)中包括的颗粒和/或细胞。在一些应用中,系统200可操作用于基本上无颗粒的气相流体或者液相流体。
图3描绘了根据例示性实施例用于执行流式细胞术的方法的操作。方法300从操作301开始,其中提供了光流体系统204。此处继续参考图2以及参考图4-10对方法300进行描述。
光流体系统204是包括流体流动系统212和检测系统214的单片集成系统。检测系统214包括基于表面波导的激发网络216、基于表面波导的收集网络218和流体流动系统212的一部分。在下面以及关于图4-9对光流体系统204进行更详细的描述。
图4描绘了根据本发明例示性实施例的光流体系统的横截面视图的示意图。光流体系统204包括通道板402-1和402-2以及光学板404。这些板共同地限定流体流动系统212和检测系统214中的每一个。
图5描绘了用于形成光流体系统204的方法的操作。方法500从操作501开始,其中形成了通道板402-1和402-2。
通道板402-1和402-2中的每一个是通过常规方法(例如,反应性离子蚀刻(RIE)、湿化学蚀刻、喷砂法等等)形成的常规微流体通道板。通道板402-1和402-2分别地包括通道网络406-1和406-2,在常规平面处理衬底中形成它们中的每一个。通道板402-1和402-2还包括通道板与光学器件板404之间分布的通孔410和端口412以使能通道网络的彼此互连以及流体流动系统212与外部设施(流体源、废物容器等等)的互连。
典型地,对于光学系统(诸如,例示性实施例),由于熔凝硅石不呈现显著的自发荧光,因此通道板衬底由熔凝硅石制成。然而,在一些应用中,通道板衬底包括除熔凝硅石以外的材料。适合在通道板衬底中使用的材料包括,但不限于,玻璃(例如,二氧化硅、borofloat玻璃、石英、派热克斯玻璃等等)、半导体(例如,硅、碳化硅、锗、GaAs、InP等等)、金属、陶瓷、塑料、复合材料等等。
通道网络406-1和406-2中的每一个是适合于与流动通道408结合对流体224执行常规流体操作(诸如,流动分离、过滤、混合、分类等等)以及迫使流体224中的细胞以单列顺序流过流动通道408的微流体通道的系统。通道网络406-1和406-2的特定布置和功能典型的是基于应用的设计的问题。通道网络406-1和406-2、流动通道408、通孔410和端口412共同地限定流体流动系统212。
在操作502处,形成光学板404。
图6描绘了光学板404的俯视图。光学板404包括流动通道408、激发网络216、收集网络218、流动通道408和通孔410。在一些实施例中,光学板404是作为常规流式细胞仪流动室的一部分提供的元件,用以例如改善或者代替常规光激发或者收集系统。
激发网络216和收集网络218中的每一个包括多个N个表面波导(各自地称为激发波导604-i或者收集波导606-i,其中1<i<N)。尽管在例示性实施例中,N=8,但是在阅读本说明书之后,本领域技术人员应当清楚,如何指定、形成和使用本发明的替换实施例,其中N等于任何实际数字以及可以小至一。此外,本领域技术人员将认识到激发网络216和收集网络218可以包括不同数量的表面波导。
在例示性实施例中,将收集波导606设置在位于区域602中的激发波导604之上的平面中。在一些实施例中,不在激发波导之上设置收集波导606。此外,在一些实施例中,激发波导604位于收集波导606的平面之上的平面中。更进一步地,在一些实施例中,激发波导604和收集波导606中的至少一些位于相同平面中。在其它实施例中,多个激发波导604和收集波导606中的至少一个分布在两个或者更多个波导层之间。
图7A-B描绘了光学板404的区域602的俯视图和横截面视图。区域602提供流动通道408、激发波导604-1至604-8以及收集波导606-1至606-8的细节图。在区域602内,在衬底608上形成激发波导604和收集波导606以使得以基本上环形的布置围绕流动通道408的中心布置它们的端面。在阅读本说明书之后,本领域技术人员应当认识到,由激发波导604和收集波导606的端面围绕的流动通道408的区域基本上限定检测区414。
图8描绘了适用于形成光学板404的子操作。操作502从子操作801开始,其中在衬底608的顶表面上形成芯层702。
衬底608是类似于上面描述的通道板衬底的平面衬底以及在例示性实施例中包括熔凝硅石以阻止自发荧光。然而,在一些实施例中,衬底608可以包括如上面讨论的以及关于通道板402-1和402-2的另一个材料。如所指示的,衬底608限定大致位于x-y平面中的衬底平面610。
芯层702是使用低压化学气相沉积(LPCVD)沉积在衬底608顶表面上的常规平面化学计量氮化硅层。芯层702具有大约25纳米(nm)的厚度以及限定波导平面704。在一些实施例中,芯层702具有不同厚度。在一些实施例中,芯层702包括除氮化硅以外的材料。适合在芯层702中使用的材料包括激发信号可以传播通过的任何材料。在一些实施例中,用不同的合适成型工艺形成芯层702。
在一些实施例中,衬底608包括表面层(诸如氧化硅),起由芯层702形成的波导的下包覆层的作用。
在操作802处,以常规方式对芯层702进行图案化以限定波导芯706-1至706-8(共同地称作波导芯706)。典型地,通过光刻法和RIE对芯层702进行图案化。对波导芯706进行图案化以使得各自具有大约1微米至大约4微米范围内以及典型地大约2微米的宽度。因此,波导芯706中的每一个限定适合于在激发光210中包括的光的波长下单模工作的条形波导。波导芯706中的每一个包括端面708,以基本上环形的布置围绕检测区414布置多个端面708。
在一些实施例中,波导芯706中的至少一个包括不同材料,具有不同波导类型和/或具有与表面波导芯706中的另一个表面波导芯不同的尺寸(即,厚度或者宽度)。不同芯材料、类型和/或尺寸使能优选用于例如不同波长、多种功能(例如,为检测区414提供光或者从检测区414收集光等等)等等的表面波导。因此,在一些实施例中,重复操作801和802中的至少一个一次或者多次。
图9A描绘了在限定波导芯706之后区域602的俯视图的示意图。
在操作803处,以常规方式形成中间包覆710。中间包覆710是通过LPCVD沉积的二氧化硅层。典型地,在形成之后,通过化学机械抛光或者另一个合适平坦化技术使中间包覆710平坦化。中间包覆710具有典型地在大约1微米至大约30微米的范围内的厚度。中间包覆710起激发波导604的上包覆和检测波导606的下包覆两者的作用。
本领域技术人员应当认识到中间包覆710的厚度是设计的问题以及基于若干因素,诸如激发网络216与收集网络218之间的串扰的可接受程度、激发和收集波导中的损耗的可接受程度等等。
在一些实施例中,通过另一个沉积技术(诸如,等离子体增强化学气相沉积(PECVD)、溅射、旋涂玻璃沉积等等)形成中间包覆710。在一些实施例中,中间包覆710包括除二氧化硅以外的材料。本领域技术人员应当认识到中间包覆710的材料的选择基于许多因素,包括光的波长、衬底608以及芯层702和712的材料、与流体224的材料相容性等等。
在操作804处,在中间包覆710上形成芯层712。芯层712类似于上面描述的芯层702;然而,形成芯层712以使得它具有大约100nm的厚度。芯层712限定波导平面716。
在操作805处,以常规方式对芯层712进行图案化以限定条形波导芯714-1至714-8(共同地称作波导芯714),它们共同地限定波导平面716。波导平面716与衬底平面610基本上平行。典型地,通过光刻法和RIE对芯层712进行图案化。
为了便于从检测区414收集光,对波导芯714进行图案化以使得它们具有大约1微米至大约4微米的范围内以及典型地大约2微米的宽度。因此,波导芯714中的每一个起用于所收集光220中的光的波长的多模波导芯的作用。如波导芯706一样,波导芯714具有端面718,以基本上环形的布置围绕检测区414布置。在一些实施例中,波导芯714具有不同宽度或者高度。
此处提供的波导芯706(和/或波导芯714)的尺寸仅仅是示例性的。本领域技术人员应当认识到波导的具体尺寸取决于系统和应用考虑,以及这些波导的任何合适的尺寸都在本发明的范围内。
此外,如上面关于波导芯706讨论的,在一些实施例中,波导芯714中的至少一个包括不同材料,具有不同波导类型和/或具有与表面波导芯714中的另一个表面波导芯不同的尺寸(即,厚度或者宽度)。不同芯材料、类型和/或尺寸使能优选用于例如不同波长、多种功能(例如,为检测区414提供光或者从检测区414收集光等等)等等的表面波导。因此,在一些实施例中,重复操作804和805中的至少一个一次或者多次。
图9B描绘了在限定波导芯714之后区域602的俯视图的示意图。
在操作806处,在波导芯714上形成上包覆层720以完成收集波导606的形成。上包覆层720类似于中间包覆层710。
应当注意,在操作806的末尾,波导芯706和714中的每一个延伸穿过周界902,该周界902限定如将在操作807中形成的广度流动通道408。由于端面由用于形成流动通道的深RIE工艺形成,因此这确保一旦流动通道形成则多个端面708和718中的每一个将以环形模式布置在流动通道的边缘处。在一些实施例中,至少一个表面波导的端面没有在形成流动通道408的操作期间形成。在一些实施例中,端面708和718中的一个或者多个在其相应芯层被图案化以限定其对应波导芯时形成。
尽管例示性实施例包括起单模波导作用的激发波导和起多模波导作用的收集波导,但是在阅读本说明书之后,本领域技术人员应当清楚,如何指定、形成和使用包括起多模波导作用的至少一个激发波导和/或起单模波导作用的至少一个收集波导的本发明的替换实施例。
在一些实施例中,使收集波导606各自地路由至衬底608的边缘以及独立地检测收集波导606。这种布置可以例如使能角度相关的散射信息的维护。
在操作807处,穿过衬底608的厚度以及其表面层形成流动通道408。流动通道408具有大约20微米至大约120微米的范围内的直径,以及典型地大约40微米,这限制流体224中的细胞单列流过检测区414。应当注意,本发明适用于除流式细胞术以外的应用,其中流动通道408的大小并不一定限制流体224中的颗粒或者细胞的大小。因此,本领域技术人员应当认识到流动通道408的直径是基于应用的设计考虑的问题。
尽管在例示性实施例中,通过常规深RIE形成流动通道408,但是,在阅读本说明书之后,本领域技术人员应当清楚,如何指定、形成和使用通过不同工艺(诸如,喷砂、激光烧蚀、湿蚀刻等等还适合于根据系统200中使用的材料形成流动通道)形成流动通道408的替换实施例。
现在返回方法500,在操作503处,通道板402-1和402-2与光学板404接合在一起使得通道网络406-1和406-2与流动通道408流体地耦合。在例示性实施例中,使用晶片键合技术(诸如,熔融键合、热阳极键合等等)接合板以使三个板熔融成单个单片元件。在一些实施例中,通过另一个合适的方法(诸如,夹紧等等)接合板。在一些实施例中,使用中间元件(诸如,O形环、垫片、沉积材料(例如,聚酰亚胺、SU-8、PMMA等等)等等)在每个板上的流体元件之间形成流体密封。
在操作504处,端口414与外部流体系统(诸如,流体224的储存器、泵浦系统和废物容器)流体地耦合。
在操作505处,激发网络与光源202光学地耦合。
光源202是提供具有适合于激发操作流式细胞仪200期间使用的整个托盘的荧光染料的波长的激发光的常规多光谱光源。在一些实施例中,光源202包括多个发光器件和/或光谱过滤器,诸如激光器、发光二极管(LED)、超发光二极管等等。
在操作506处,收集网络与检测器206光学地耦合。
检测器206是可操作用于检测从光流体系统204接收的所收集的光220中包括的波长中的一个或者多个的常规检测系统。检测器206包括多个检测器和波长滤波器,适合于辨别由收集网络216收集的荧光信号和散射信号。检测器206向处理器208提供输出信号222。
处理器208是可操作用于接收输出信号222以及进行输出信号分析以估计流体224和/或细胞226的一个或者多个参数的常规处理系统。
现在返回方法300,在操作302处,通过光流体系统212将流体224从储存器228泵送到废物容器230,使得其组成细胞226沿着流动方向724流过检测区414。如图7B描绘的,流动方向724与z方向对准,z方向与衬底平面610以及波导平面704和716中的每一个正交。在一些实施例中,流动方向724不与波导平面704和716正交;然而,应当注意,流动方向724既不与波导平面中的任何一个平行又不与波导平面中的任何一个共面是本发明的方面。
在操作303处,光源202向光流体系统204提供光信号210。
在操作304处,用激发光210询问细胞226。
图10描绘了询问细胞226期间的检测区414的侧视图。由激发波导604向细胞226提供激发光。
用激发光210询问细胞226导致输出光1002,包括如上面讨论的前向散射光、侧面散射光和荧光信号。
在操作305处,收集波导606捕获输出光1002的一部分作为所收集的光220。
在操作306处,收集波导606将所收集的光220输送至检测器206,该检测器206将其转换成输出信号222。
在操作307处,处理器208执行输出信号222的分析以及提供细胞226的感兴趣参数的估计。
图11描绘了根据本发明第一替换实施例的区域602的俯视图的示意图。系统1100类似于上面描述的系统200;然而,系统1100包括布置成阵列的激发波导和收集波导对,共同地形成围绕流动通道408的多边形布置。
如上所述以及关于图7A-B,每个波导对1102包括一个激发波导604和一个收集波导606。
波导对1102布置成波导阵列1104-1至1104-8(共同地称为波导阵列1104),它们中的每一个包括以线性方式布置的八个波导对。波导阵列1104形成与流动通道408同中心的八边形布置。尽管在所示示例中,波导阵列1104形成具有八个边的多边形,但是在阅读本说明书之后,本领域技术人员应当清楚,如何指定、形成和使用波导阵列1104形成具有任何实际数量的边的多边形的替换实施例。此外,本领域技术人员应当认识到,波导阵列1104可以包括任何实际数量的波导对。
波导阵列1104围绕流动通道408的布置产生具有基本上圆形横截面的检测区1106。在一些实施例中,检测区1106具有除了圆形以外的横截面形状。
图12A-C描绘了对于不同波长的激发光跨越检测区的直径的模拟照射图案。
图案1200、1202和1204示出了分别地对于404nm、532nm和632nm的波长的TM偏振光跨越120微米直径流动通道的照射图案。
图13A-C描绘了对于不同波长的激发光的整个检测区1106上的随机相位场分布的曲线图。
曲线图1300、1302和1304描绘了分别地对于404nm、532nm和632nm的波长的TE偏振光跨越160微米直径流动通道的光功率分布。
图12和图13表明根据第一例示性实施例可以通过提供来自八边形图案的波导阵列的激发光以实现基本上均匀的照射。
尽管上面描述的波导布置使能流动通道区域的照射的显著提高,但是由围绕区域的小面的布置仅仅确定任何波长的照射图案但在操作期间它们是不可控制的。然而,在使用期间使能对照射图案形状的控制将是合乎需要的。
本发明的另一个方面是可以通过控制通过一个或者多个激发波导进入检测区414中的光的相位和/或幅度以获得对检测区中的照射图案的控制。在一些实施例中,这使波束成形能够提供在检测区414内的离散位置处具有局部强度最大值的特定照射图案。
此外,还可以通过控制单个收集波导中的光信号的相位以提高由该波导捕获的光信号的识别。
在一些实施例中,收集波导606中的至少一个是包括偏振滤光器的单模波导。此外,在这些实施例中的一些中,所提供的激发光210是偏振的(例如,如TM光)。在这种配置中,如N.G.Khlebtsov等人在“Can the Light Scattering Depolarization Ratio of Small Particles Be Greater Than 1/3?”(J.Phys.Chem.B,Vol.2005,No.109,pp.13578-13584(2005))(其通过引用合并于此)中描述的,本发明使能部分转换为另一个偏振模式(例如,TE)的光的检测,其提供关于颗粒形状的指示(例如,直径对比长度的比率等等)。
图14描绘了根据本发明第二替换实施例的光学板。光学板1400类似于光学板404以及包括所有相同结构;然而,光学板1400还包括相位控制元件1402-E-1至1402-E-8以及相位控制元件1402-C-1至1402-C-8(分别共同地称为PCE 1402-E和PCE 1402-C)。相位控制元件1402-E和1402-C中的每一个与激发波导或者收集波导操作地耦合,使得其可以控制传播通过波导的光信号的相位。
图15A和和15B分别地描绘了根据本发明第二替换实施例的相位控制元件1402-E-i和1402-C-i的横截面视图。相位控制元件1402-E-i和1402-C-i中的每一个包括与其相应波导芯操作地耦合的应变元件1502。应变元件1502包括下电极1504、压电层1506和上电极1508。
下电极1504和上电极1508中的每一个是一层电气导电材料,诸如铂、金、铝等等。下电极1504和上电极1508的厚度是设计选择的问题。
压电层1506是具有厚度t的一层压电材料,诸如锆钛酸铅(PZT)。使压电层1506图案化以形成基本上矩形的区域,在该区域上形成上电极1508。本领域技术人员应当认识到,上电极1508的宽度w和长度L(其中w是沿着横向于其下层波导的轴向方向的方向的层的维度以及L是沿着其下层波导的周向方向的维度)有效地限定应变元件1502的可操作维度。如下面以及关于图16讨论的,PCE 1402-E和PCE 1402-C的操作特征基于t、w和L的值。
在一些实施例中,压电层1506和下电极1504中的一个或者两者没有被图案化以及因此保留在衬底的整个表面上。在这种实施例中,穿过压电材料形成通孔以使能与下面的下电极建立电接触。
在PCE 1402-E-i中,在已经在图案化收集波导芯714期间去除了芯层712的区域中的中间包覆710上设置应变元件1502。
在PCE 1402-C-i中,在已经在图案化激发波导芯706期间去除了芯层702的区域中的上包覆722上设置应变元件1502。
处理器208为PCE 1402-E-i和PCE 1402-C-i中的每一个分别地提供控制信号1510-E-i和1510-C-i。这些控制信号在下电极1504与上电极1508之间施加电压差,其引起压电层1506中的应变。该应变传输到下层波导芯中,引起其有效折射率的变化。
以类似的方式,由处理器208提供的控制信号1508-C-i控制传播通过收集波导606-i的光的相位。控制信号1508-C-i是施加至如图所示设置在上包覆722上的下电极1504和上电极1508的电压差。对PCE 1402-C-i的电极施加电压差引起压电层1506中的应变,该应变传输到波导芯714-i中,引起其折射率的改变。
图16描绘了根据压电层1506的厚度以及上电极1508的长度L和宽度w的激发波导芯706-i的有效折射率的变化的模拟结果。
曲线图1600示出了对于具有0.5微米的厚度和13.99mm的上电极长度的压电层1506,根据上电极宽度w的激发波导芯706-i的折射率变化。
曲线图1602示出了对于具有1.0微米的厚度和7.66mm的上电极长度的压电层1506,根据上电极宽度w的激发波导芯706-i的折射率变化。
曲线图1604示出了对于具有1.5微米的厚度和5.51mm的上电极长度的压电层1506,根据上电极宽度w的激发波导芯706-i的折射率变化。
曲线图1606示出了对于具有2.0微米的厚度和4.45mm的上电极长度的压电层1506,根据上电极宽度w的激发波导芯706-i的折射率变化。
曲线图1600至1606示出了可以在与应变元件1502操作耦合的波导芯中实现折射率的显著变化,其将引起传播通过波导的光信号的相位的相应变化。
本领域技术人员应当认识到基于压电层的PCE 1042仅仅是本发明范围内的相位控制元件的一个示例。例如,可以通过热光学调制(即,通过波导上设置的加热器)、使用磁致伸缩元件的双折射调制等等以控制相位。此外,在一些实施例中,通过使用幅度调制器(诸如,马赫-策恩德尔干涉仪结构)控制通过一个或者多个激发波导进入的光的幅度以提供对检测区中的照射图案的控制。
在一些实施例中,激发波导604中的至少一些包括相位和/或幅度控制器,使得激发波导可操作用于控制围绕检测区414的照射图案。因此,单个固定位置的收集波导可以用于从检测区收集散射光/荧光。在某些情况下,这提供更简单的检测方案和/或使能单个大的并且灵敏的检测器(例如,雪崩光电二极管、光电倍增管等等)APD的使用以检测太弱而不能用常规检测器阵列收集的输出光信号。通过使所检测的光与所控制的照射图案的方向相关,保持角度信息。
图17描绘了根据现有技术的常规流式细胞仪流动单元的图片。流动单元1700包括单元主体1702、通道1704、流体端口1706以及透镜1708。
穿过单元主体1702的长度形成通道1704以使得其限定用于将流体输送通过检测区414的长管道。检测区414由透镜1708的位置限定,该透镜1708集成到流动单元以使得其将自由空间激发光聚焦到检测区中以及从检测区收集光(例如,前向散射光和侧面散射光以及荧光信号)。
图18A-B描绘了根据本发明第三替换实施例的流式细胞术流动单元。流动单元1800表示具有与现有技术流动单元基本上相同形状因子但提供改进的光学系统性能和更简单的操作的本发明实施例。流动单元1800包括单元主体1802、通道1804、流体端口1706和光流体系统1806。
单元主体1802类似于单元主体1702;然而,单元主体包括两个常规单元主体部分1702-1和1702-2,附接至光流体系统1806的两侧。典型地,单元主体部分1702-1和1702-2通过常规接合技术(诸如,熔融键合、胶等等)与光流体系统1806接合在一起。单元主体部分1702-1以及1702-2包括通道1704的区段,该区段隔挡(bookend)以及流体地耦合流动通道408以共同地限定通道1804。
光流体系统1806类似于光学板404以及包括板1808和检测系统1812,该检测系统1812包括激发网络1814、收集网络1816和流动通道408。激发网络1814和收集网络1816类似于激发网络216和收集网络218以及在波导平面1810中形成,该波导平面1810由板1808的顶表面限定。
应当注意,在相同波导平面中形成激发网络1814和收集网络1816的波导。因此,围绕流动通道408的一侧布置所有激发波导,而围绕流动通道的另一侧布置所有收集波导。尽管由这种布置提供的照射图案不像本发明的一些其它实施例那么均匀,但是该照射图案仍然典型地示出相对于由现有技术流式细胞仪布置(例如,系统1700所示的流式细胞仪布置)提供的照射图案的显著提高。在一些实施例中,在如上所述的两个或者更多个波导平面中设置激发网络1814和收集网络1816的波导。此外,在一些实施例中,以另一个布置(诸如,上面描述的那些布置)围绕流动通道408布置激发网络1814和收集网络1816的波导。
本领域技术人员应当认识到,有若干方式光学地耦合至激发网络1814和收集网络1816以及从激发网络1814和收集网络1816耦合,诸如使光纤对接耦合至波导网络、将自由空间光信号聚焦到网络的端面中等等。
应当理解,本公开教导了例示性实施例的仅一个示例以及在阅读本公开之后本领域技术人员可以容易的想出本发明的许多变型以及本发明的范围将由下列权利要求决定。
- 还没有人留言评论。精彩留言会获得点赞!