单胺抗帕金森药物的双羟萘酸盐、其制备方法及其用途与流程
相关申请的交叉引用
本申请要求在2017年8月17日提交的美国临时申请号62/546,984的权益,其内容通过引用整体并入本文。
在各实施方案中,本发明概括而言涉及抗帕金森病药的双羟萘酸盐,例如罗替戈汀、罗匹尼罗、普拉克索、司来吉兰、雷沙吉兰和/或沙芬酰胺的双羟萘酸盐,包含这类盐的药物组合物,制备这类盐的方法,以及用这类盐和组合物治疗有需要的受试者的方法。
背景
帕金森病(pd)是神经系统的运动系统障碍。其特征为进行性疾病,其影响运动并导致产生多巴胺的脑细胞的损失,引起手、臂、腿、颌和脸的震颤和/或四肢和躯干的强直或僵硬。主要症状包括肌肉僵硬、运动缓慢、静止震颤和姿势不稳定。
最常见的抗帕金森病药物是替代脑中多巴胺水平、模拟多巴胺的作用或减缓/抑制脑中多巴胺的降解。多巴胺能药物的主要类别包括多巴胺激动剂,例如罗替戈汀、罗匹尼罗和普拉克索,其化学结构如下所示。来自单胺氧化酶-b(mao-b)抑制剂类的药物,例如司来吉兰、雷沙吉兰和沙芬酰胺(参见下面的化学结构),通过阻断多巴胺的代谢来增加基底神经节中的多巴胺水平。这些药物抑制mao-b,后者分解由多巴胺能神经元分泌的多巴胺。mao-b活性的降低导致神经系统中l-dopa增加,从而减轻pd的症状。
目前可用的多巴胺激动剂和mao-b抑制剂的pd治疗通常提供每日口服施用。然而,需要抗pd药物的更好的给药方案,其可以例如增加患者的依从性和/或减少副作用。
发明概述
在多个实施方案中,本发明提供了多种不同的固态形式,例如抗帕金森病药的双羟萘酸盐,例如单胺抗帕金森病药(下文称作“单胺药物”),其为新多晶型物形式,更特别地提供了罗替戈汀的双羟萘酸盐、罗匹尼罗的双羟萘酸盐、普拉克索的双羟萘酸盐、司来吉兰的双羟萘酸盐、雷沙吉兰的双羟萘酸盐和/或沙芬酰胺的双羟萘酸盐。在一些实施方案中,本发明还提供了包含一种或多种所述盐的药物组合物,制备所述盐的方法,以及用一种或多种所述盐和药物组合物治疗有需要的受试者或患者(例如人)的方法。在一些实施方案中,本发明还提供了具有长效和/或延长释放特性的包含一种或多种单胺药物的双羟萘酸盐的制剂。在本文所述的任何实施方案中,单胺药物可以是罗替戈汀、罗匹尼罗、普拉克索、司来吉兰、雷沙吉兰和/或沙芬酰胺。在本文所述的任何实施方案中,单胺药物还可以是罗匹尼罗、普拉克索或罗替戈汀。
在一些实施方案中,本发明提供了单胺药物的新的双羟萘酸盐,例如不同多晶型物形式的双羟萘酸盐。在一些实施方案中,单胺药物的游离碱与双羟萘酸的摩尔比为约1:1(在本文中称为单胺药物的单-双羟萘酸盐)。在一些实施方案中,单胺药物的游离碱与双羟萘酸的摩尔比为约2:1(其在本文中称为单胺药物的半双羟萘酸盐)。在一些实施方案中,单胺药物的双羟萘酸盐是(1)结晶的,包括无水、水合物、溶剂化物形式及其多晶型物,或(2)无定形的。在一些实施方案中,上述盐在制备制剂中尤其有用,例如缓释制剂(或组合物),其中释放速率最低限度地依赖于注射部位的环境ph。
在一些实施方案中,本发明提供了药物组合物,其包含单胺药物的双羟萘酸盐和至少一种药学上可接受的载体。在一些实施方案中,载体是粘性水性或非水性载体。
在一些实施方案中,本发明提供了一种制备单胺药物的双羟萘酸盐的方法,包括在溶剂中用双羟萘酸处理或混合单胺药物,或者在溶剂中用双羟萘酸盐处理或混合单胺药物的盐。
在一些实施方案中,本发明提供了治疗患有与帕金森病相关的综合征的患者的方法,包括向需要治疗的患者施用治疗有效量的单胺药物的双羟萘酸盐或包含单胺药物的双羟萘酸盐和至少一种药学上可接受的载体的药物组合物。在一些实施方案中,组合物通过注射施用。在一些具体实施方案中,组合物肌内或皮下施用。
在一些实施方案中,本发明提供了制剂(或组合物),其包含作为活性成分或活性剂的单胺药物的双羟萘酸盐,以及一种或多种药学上可接受的载体。在一些实施方案中,制剂(或组合物)可以满足对于具有受控和/或持续释放速率的、稳定的、药学上合适的制剂的未满足的需要,所述制剂可以用作贮库制剂或用于肌内或皮下使用。
本公开的另外的实施方案和优点将部分地在以下描述中阐述,并且将从描述中得出,或者可以通过本公开的实践而获知。应当理解,前面的概述和下面的详细描述都仅仅是示例性和解释性的,而不是对所要求保护的本发明的限制。
附图简述
在此仅通过示例的方式,参考附图描述本发明的一些实施方案。现在通过具体详细参考附图,强调的是所示的细节是作为示例的,并且是为了说明性地讨论本发明的实施方案。
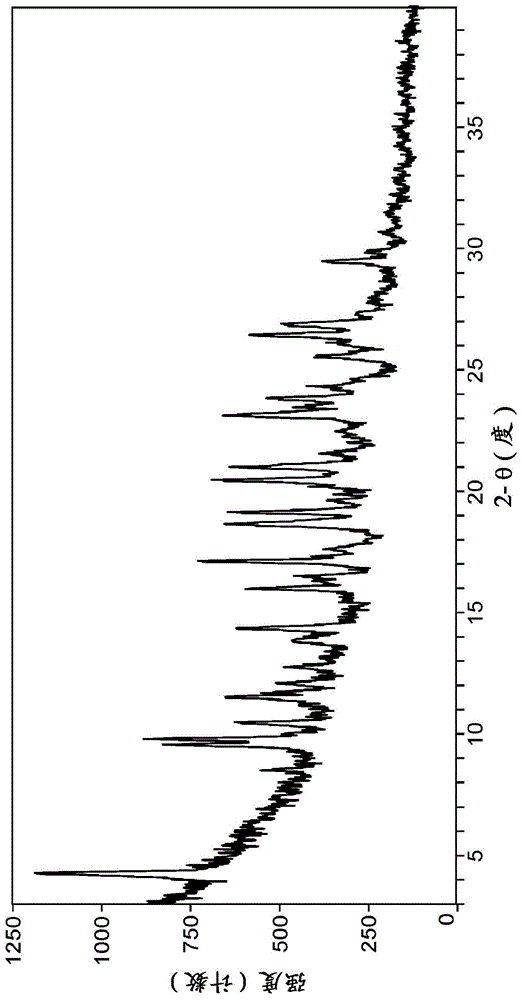
图1描述了从dmso和水的混合物获得的罗匹尼罗的双羟萘酸盐晶型a(罗匹尼罗与双羟萘酸的摩尔比为1:1)的x-射线粉末衍射(“xrpd”)谱。
图2描述了由dmso和水的混合物获得的罗匹尼罗的双羟萘酸盐晶型a(罗匹尼罗与双羟萘酸的摩尔比为1:1)的差示扫描量热法(“dsc”)热分析图。
图3描述了罗匹尼罗的双羟萘酸盐晶型b(罗匹尼罗与双羟萘酸的摩尔比为1:1)的xrpd谱图,该晶型b是通过在170℃加热图1和2中描述的物质30分钟而获得的。
图4描述了罗匹尼罗的双羟萘酸盐晶型b(罗匹尼罗与双羟萘酸的摩尔比为1:1)的dsc热分析图,该晶型b是通过在170℃加热图1和2中描述的物质30分钟而获得的。
图5描述了从乙醇、水和peg6000的混合物获得的罗匹尼罗的双羟萘酸盐晶型c(罗匹尼罗与双羟萘酸的摩尔比为2:1)的xrpd谱图。
图6描述了从乙醇、水和peg6000的混合物获得的罗匹尼罗的双羟萘酸盐晶型c(罗匹尼罗与双羟萘酸的摩尔比为2:1)的dsc热分析图。
图7描述了从dmso和乙腈的混合物获得的罗匹尼罗的双羟萘酸盐晶型d(罗匹尼罗与双羟萘酸的摩尔比为1:1)的xrpd谱图。
图8描述了从dmso和乙腈的混合物获得的罗匹尼罗的双羟萘酸盐晶型d(罗匹尼罗与双羟萘酸的摩尔比为1:1)的dsc热分析图。
图9描述了从乙醇、水和聚(烯丙胺盐酸盐)的混合物获得的罗匹尼罗的双羟萘酸盐晶型e(罗匹尼罗与双羟萘酸的摩尔比为2:1)的xrpd谱图。
图10描述了从乙醇、水和聚(烯丙胺盐酸盐)的混合物获得的罗匹尼罗的双羟萘酸盐晶型e(罗匹尼罗与双羟萘酸的摩尔比为2:1)的dsc热分析图。
图11描述了从乙醇、丙酮和正庚烷的混合物获得的罗替戈汀双羟萘酸盐晶型i(罗替戈汀与双羟萘酸的摩尔比为1:1)的xrpd图谱。
图12描述了从乙醇、丙酮和正庚烷的混合物获得的罗替戈汀双羟萘酸盐晶型i(罗替戈汀与双羟萘酸的摩尔比为1:1)的dsc热分析图。
图13描述了从丙酮和水的混合物获得的普拉克索双羟萘酸盐晶型1(普拉克索与双羟萘酸的摩尔比为1:1)的xrpd谱图。
图14描述了由丙酮和水的混合物获得的普拉克索双羟萘酸盐晶型1(普拉克索与双羟萘酸的摩尔比为1:1)的dsc热分析图。
图15描述了由丙酮和甲醇混合物获得的普拉克索双羟萘酸盐晶型2(普拉克索与双羟萘酸的摩尔比为1:1)的xrpd图谱。
图16描述了由丙酮和甲醇混合物获得的普拉克索双羟萘酸盐晶型2(普拉克索与双羟萘酸的摩尔比为1:1)的dsc热分析图。
图17描绘了从乙酸乙酯溶液获得的普拉克索双羟萘酸盐晶型3(普拉克索与双羟萘酸的摩尔比为2:1)的xrpd谱。
图18描述了从乙酸乙酯溶液获得的普拉克索双羟萘酸盐晶型3(普拉克索与双羟萘酸的摩尔比为2:1)的dsc热分析图。
图19描绘了从四氢呋喃溶液获得的普拉克索双羟萘酸盐晶型4(普拉克索与双羟萘酸的摩尔比为2:1)的xrpd谱。
图20描述了从四氢呋喃溶液获得的普拉克索双羟萘酸盐晶型4(普拉克索与双羟萘酸的摩尔比为2:1)的dsc热分析图。
图21描述了从丙酮和水的混合物获得的普拉克索双羟萘酸盐(普拉克索与双羟萘酸的摩尔比为1:1)的1h-nmr谱。
图22描述了从四氢呋喃溶液获得的普拉克索双羟萘酸盐(普拉克索与双羟萘酸的摩尔比为2:1)的1h-nmr谱。
图23描述了从实施例1中获得的罗匹尼罗的双羟萘酸盐(罗匹尼罗与双羟萘酸的摩尔比为1:1)的1h-nmr谱。
图24描述了从实施例3得到的罗匹尼罗的双羟萘酸盐(罗匹尼罗与双羟萘酸的摩尔比为2:1)的1h-nmr谱。
图25描述了从实施例6获得的罗替戈汀双羟萘酸盐(罗替戈汀与双羟萘酸的摩尔比为1:1)的1h-nmr谱。
图26描述了从实施例9中获得的普拉克索双羟萘酸盐(普拉克索与双羟萘酸的摩尔比为2:1)的1h-nmr谱。
发明详述
在描述本发明的各实施方案的细节之前,应当理解,本发明在其应用方面不限于在以下描述中阐述的细节构造和构成安排。本发明能够由其它实施方案实施,并且能够由本领域技术人员以各种方式实践或执行。
还应特别理解,本文中所述的任何数值包括从较低值到较高值的所有值,即,所列举的最低值和最高值之间的数值的所有可能组合应被认为在本申请中明确地说明了。
目前可用的多巴胺激动剂和mao-b抑制剂的pd治疗通常提供每日口服施用。例如,普拉克索,一种在过去十年广泛使用的多巴胺激动剂,作为用于患有早期帕金森病的患者以及患有更晚期疾病的患者的单一疗法,每天施用三次或每天施用一次。不幸的是,在帕金森病进程中运动和非运动并发症的发展代表了目前治疗管理的主要挑战(m.senek,d.nyholm,cnsdrugs.28(1):19-27,2014)。在疾病晚期,患者经常经历pd症状-例如运动迟缓-和动作障碍,这响应于药物浓度的波动。研究表明,连续输注多巴胺激动剂或经肠输注左旋多巴降低了药物动力学和运动功能二者的这种波动。这些研究表明,连续递送抗pd药物如多巴胺激动剂将提供显著的益处,减轻运动和非运动并发症。为了达到这些目的,人们已努力开发连续施用制剂,例如罗替戈汀的透皮递送和阿扑吗啡的连续皮下输注,以提供更连续的药物浓度、持续的益处和最小化的副作用。然而,这些方案远不是最佳的,仅提供每日短持续时间的连续药物浓度。此外,超过24小时的长期释放方案也将帮助患者依从,因为患有晚期pd的患者通常不顺从,使得难以评估患者是否已接受适当剂量的药物。总之,开发长于24小时的连续药物递送制剂(例如延长释放7天)以更好地减轻pd患者的运动和非运动并发症仍然是存在显著的益处和未满足的医疗需求。
单胺抗pd药物是弱有机碱。在碱性溶液(高ph)中,它们以游离碱形式存在。单胺药物的水溶解度随着溶液ph的降低而增加,这是由于增加的离子化的药物部分。在高浓度的离子化药物(质子化胺)情况下,由于超过溶度积(ksp),盐形式将沉淀出来。药物和抗衡离子的性质决定了ksp和盐的相关固态性质。
有很多种抗衡离子用以使用无机和有机酸来制备碱的盐。形成碱性药物的盐的最常用的阴离子是盐酸盐形式。例如,requipxl,口服多巴胺激动剂罗匹尼罗的缓释片剂和市售产品是盐酸盐。罗匹尼罗的透皮贴剂也使用其盐酸盐作为活性药物成分(api)(chen等人的美国专利号5807570)。在缓释片剂中,将普拉克索二盐酸盐单水合物分散于包含亲水性聚合物的基质中以实现24小时释放(friedl等人的美国专利号7695734和amidon等人的美国专利号8399016)。使用普拉克索的苯磺酸盐作为替代的药物活性剂也已在eupen等人的美国专利号7365086中描述。贮库形式的盐酸罗替戈汀的施用已描述于rimpler等人的美国专利号8604076中,贮库方案旨在向患者施用后至少24小时的期间内提供治疗上显著的罗替戈汀血浆水平。制备这些单胺药物的盐以改善物理性质,包括稳定性、溶解性或增加施用的溶出速率。选择相应的盐使它们具有即释或缓释剂型的理想性质。然而,这些制剂,即使是缓释形式,也要在不超过24小时被施用。因此,一个目的是提供比目前24小时施用间隔显著更不频繁地递送单胺药物的改进方法,并且可以成本有效的方式制备制剂。
本发明人已发现,需要将单胺药物配制在例如贮库制剂中,或者配置为注射制剂如肌内或皮下制剂,以通过维持持续和连续的药物物质浓度确保药物的一致和适当剂量、和使临床益处最大化,并改善患者的顺应性。
已知肌肉组织的ph可随运动、应激和损伤而波动,这可影响药物溶解度,并因此影响可注射药物的吸收速率。因此,在一些实施方案中,还符合需要的是,开发一种注射缓释制剂,其中活性成分的释放速率最小程度地依赖于ph波动,如与运动、应激和/或损伤相关的那些ph波动。
在一些实施方案中,本发明人发现固态或固体形式的抗帕金森病药如单胺抗帕金森病(抗pd)药物双羟萘酸盐可以是有利的。优点之一是,在合适的制剂中的具有特定多晶型形式和粒度分布的单胺药物的双羟萘酸盐可提供所需的长效的和/或缓释的特性。所述单胺药物的双羟萘酸盐可提供治疗患有帕金森病(pd)的患者的替代的和更理想的给药方案。与现有的口服药物产品相比,通过提供药物的连续递送它还具有更优异的药物吸收和分布特性,其将在施用间隔期间维持稳定的血药浓度并降低最大与最小血药浓度比,从而最终改善安全性并提高临床有效性。
双羟萘酸的化学结构为:
双羟萘酸的分子量为388g/mol,pka1为2.51,且pka2为3.1。关于双羟萘酸的化学结构,两个羧基抗衡离子都可以与单胺药物的胺形成盐,导致单胺药物与双羟萘酸的摩尔比为约1:1或约2:1,如图1-20中所说明的那些。
在一个实施方案中,本发明提供了抗pd药物如单胺抗pd药物的双羟萘酸盐以及含有所述双羟萘酸盐的组合物和制剂。优选双羟萘酸盐的特征在于单胺药物与双羟萘酸的摩尔比为约1:1或约2:1。双羟萘酸盐可以是结晶的、无水的、水合的、溶剂化的或无定形的。
在另一个实施方案中,本发明提供了罗匹尼罗的双羟萘酸盐,例如罗匹尼罗的双羟萘酸盐的五种晶形,晶形a至晶形e。罗匹尼罗的双羟萘酸盐的晶形a、b和d各自具有约1:1的罗匹尼罗与双羟萘酸的摩尔比,而罗匹尼罗的双羟萘酸盐的晶形c和e各自具有约2:1的罗匹尼罗与双羟萘酸的摩尔比。罗匹尼罗的双羟萘酸盐可以由本领域技术人员根据本发明公开的内容制备,参见例如实施例部分。例如,罗匹尼罗的双羟萘酸盐的a、b、c、d、e型可分别按照实施例部分的实施例1-5中所述的方法制备。
在一些实施方案中,罗匹尼罗的双羟萘酸盐的晶型a至晶型e的特征在于具有一种或多种以下性质:(1)对于每种晶型,分别具有与图1、3、5、7、9中显示的一个或多个(例如,两个或更多个、三个或更多个等,例如,1、2、3、4、5、6个或更多个)主峰基本上一致的(例如,在±0.2°2-θ内)、以2θ表示的3至40度的峰的x射线粉末衍射图;(2)对于每种晶型,分别与图1、3、5、7、9中所示的基本上一致的x射线粉末衍射图;(3)对于每种晶形,分别与图2、4、6、8、10中所示的那些基本上一致的差示扫描量热法热分析图;和(4)(1)、(2)和(3)的任意组合,分别就每种晶形而言。如本文所用,“主峰”是指xrpd谱(例如,如本文的图和表中所示)中的峰,其相对强度(高度)为约15%或更高,优选约30%或更高(例如,35%或更高、50%或更高、60%或更高、70%或更高、80%或更高、或90%或更高)。在一些实施方案中,“主峰”是指xrpd谱中的峰(例如,如本文的图和表中所示),其具有约80%或更高的相对强度(高度)。
例如,在一些实施方案中,罗匹尼罗的双羟萘酸盐晶型a可以通过具有以下峰中的一个或多个(例如4个或更多、6个或更多、8个或更多、10个或更多、12个或更多个、或全部)峰的xrpd谱表征:4.3、9.8、11.5、14.4、16.0、17.1、18.6、19.1、20.5、21.0、23.1、23.8、26.5和26.9,±0.2°2-θ。在一些实施方案中,罗匹尼罗的双羟萘酸盐晶形a可以通过具有以下峰中的一个或多个(例如2个或更多个、4个或更多个、6个或更多个、或全部)峰的xrpd谱表征:4.3、9.8、17.1、18.6、19.1、20.5、21.0和23.1,±0.2°2-θ。在一些实施方案中,罗匹尼罗的双羟萘酸盐晶形a可以通过具有以下峰中的一个或多个(例如1、2、3或4个)峰的xrpd谱表征:4.3、17.1、18.6和20.5,±0.2°2-θ。
在一些实施方案中,罗匹尼罗的双羟萘酸盐晶形b可以通过具有以下峰中的一个或多个(例如,4或更多个、6或更多个、8或更多个、10个或更多个、或全部)峰的xrpd谱表征:9.4、11.5、12.0、12.7、15.6、16.4、17.2、18.7、21.0、23.1、23.4和26.2,±0.2°2-θ。在一些实施方案中,罗匹尼罗的双羟萘酸盐晶形b可以通过具有以下峰中的一个或多个(例如,2或更多个、4或更多个、6个或更多个或全部)峰的xrpd谱表征:11.5、12.0、12.7、16.4、21.0、23.1、23.4和26.2,±0.2°2-θ。在一些实施方案中,罗匹尼罗的双羟萘酸盐晶形b可以通过具有以下峰中的一个或多个(例如,2或更多个、4个或更多个、或全部)峰的xrpd谱表征:11.5、16.4、21.0、23.1、23.4和26.2,±0.2°2-θ。
在一些实施方案中,罗匹尼罗的双羟萘酸盐晶形c可以通过具有以下峰中的一个或多个(例如,1、2、3或4)峰的xrpd谱表征:8.0、9.5、16.1和18.8,±0.2°2-θ。在一些实施方案中,罗匹尼罗的双羟萘酸盐晶形c可以通过在16.1和18.8,±0.2°2-θ处具有峰的xrpd谱表征。
在一些实施方案中,罗匹尼罗的双羟萘酸盐晶形d可以通过具有以下峰中的一个或多个(例如,1、2、3、4、5或6)峰的xrpd谱表征:14.3、17.9、21.5、22.4、24.8和25.2,±0.2°2-θ。在一些实施方案中,罗匹尼罗的双羟萘酸盐晶形d可以通过具有以下峰中的一个或多个(1、2或3)峰的xrpd谱表征:14.3、17.9和25.2,±0.2°2-θ,例如,罗匹尼罗的双羟萘酸盐晶形d可以通过在17.9,±0.2°2-θ处具有峰的xrpd谱表征。
在一些实施方案中,罗匹尼罗的双羟萘酸盐晶形e可以通过具有以下峰中的一个或多个(例如,4或更多个、6或更多个、8或更多个、10个或更多个、或全部)峰的xrpd谱表征:11.1、11.7、12.0、15.5、18.8、19.6、20.2、21.0、22.9、23.6、26.1和26.6,±0.2°2-θ。在一些实施方案中,罗匹尼罗的双羟萘酸盐晶形e可以通过具有以下峰中的一个或多个(例如,2或更多个、4个或更多个、或全部)峰的xrpd谱表征:11.1、11.7、12.0、21.0、26.1和26.6,±0.2°2-θ。在一些实施方案中,罗匹尼罗的双羟萘酸盐晶形e可以通过具有以下峰中的一个或多个(例如,1、2或3)峰的xrpd谱表征:11.7、12.0和21.0,±0.2°2-θ。
在一些实施方案中,罗匹尼罗的双羟萘酸盐的晶型a至晶型e中的每一种可以是基本上纯的,例如,每一种晶型可以基本上不含罗匹尼罗的双羟萘酸盐的其它晶型或无定形形式(例如,少于20%、少于10%、少于5%或用本文所述的xrpd方法检测不到)。然而,在一些实施方案中,罗匹尼罗的双羟萘酸盐的晶型a至晶型e中的每一种可以与一种或多种罗匹尼罗的双羟萘酸盐的其它结晶或无定形的形式混合存在。
在另一实施方案中,本发明涉及罗替戈汀的双羟萘酸盐,例如罗替戈汀双羟萘酸盐的晶形i,其具有摩尔比为约1:1的罗替戈汀与双羟萘酸。本领域技术人员根据本发明公开内容可制备罗替戈汀的双羟萘酸盐,参见例如实施例部分。例如,罗替戈汀双羟萘酸盐的晶型i可以通过按照实施例部分的实施例6中描述的方法制备。
在一些实施方案中,罗替戈汀双羟萘酸盐的晶形i的特征可在于一种或多种以下性质:(1)具有与图11所示的一个或多个(例如,两个或更多个、三个或更多个等,例如,1、2、3、4、5、6个或更多个)主峰基本一致的(例如,在±0.2°2-θ内)、以2θ表示的3至40度的峰的x射线粉末衍射图;(2)基本上与图11所示一致的x-射线粉末衍射图;(3)基本上与图12所示一致的差示扫描量热法热谱图;以及(4)(1)、(2)和(3)的任意组合。例如,在一些实施方案中,罗替戈汀的双羟萘酸盐晶型i可以通过具有以下峰中的一个或多个(例如,1、2、3、4、5、6、7或8)峰的xrpd谱表征:4.6、9.3、17.5、18.7、24.2、26.4、28.2和29.6,±0.2°2-θ。在一些实施方案中,罗替戈汀的双羟萘酸盐的晶型i可以通过具有在4.6和9.3,±0.2°2-θ处的两个峰或其中一个峰的xrpd谱表征。在一些实施方案中,罗替戈汀的双羟萘酸盐的晶型i可以是基本纯的,例如基本不含罗替戈汀双羟萘酸盐的其它结晶或无定形形式(例如,少于20%、少于10%、少于5%或用本文所述的xrpd方法检测不到)。然而,在一些实施方案中,罗替戈汀双羟萘酸盐的晶形i可以与罗替戈汀双羟萘酸盐的一种或多种其它结晶或无定形的形式混合存在。
在另一个实施方案中,本发明涉及普拉克索的双羟萘酸盐,例如普拉克索双羟萘酸盐的晶型,晶型1至晶型4。普拉克索的双羟萘酸盐可以由本领域技术人员根据本发明公开内容制备,参见例如实施例部分。例如,普拉克索的双羟萘酸盐的晶型1-4可以分别按照实施例部分的实施例7-10中所述的方法制备。
普拉克索双羟萘酸盐的形式1和2各具有约1:1的普拉克索与双羟萘酸的摩尔比,而普拉克索双羟萘酸盐的形式3和形式4各具有约2:1的普拉克索与双羟萘酸的摩尔比。在一些实施方案中,普拉克索的双羟萘酸盐的晶形1至4可以通过一种或多种以下性质表征:(1)对于每种晶型,分别具有与图13、15、17、19中显示的一个或多个(例如,两个或更多个、三个或更多个等,例如,1、2、3、4、5、6个或更多个)主峰基本上一致的(例如,在±0.2°2-θ内)、以2θ表示的3至40度的峰的x射线粉末衍射图;(2)对于每种晶型,分别与图13、15、17、19所示的那些基本上一致的各晶形的x-射线粉末衍射图;(3)对于每种晶型,分别与图14、16、18、20中所示的那些基本上一致的差示扫描量热法热分析图;以及(4)(1)、(2)和(3)的任意组合。
在一些实施方案中,普拉克索的双羟萘酸盐的形式1可以通过具有以下峰中的一个或多个(例如,1、2、3、4、5、6、7、8或9)峰的xrpd谱表征:7.7、11.8、13.8、15.3、18.9、21.1、23.1、23.7和26.4,±0.2°2-θ。在一些实施方案中,普拉克索的双羟萘酸盐的形式1可以通过具有以下峰中的一个或多个(例如,1、2或3)峰的xrpd谱表征:13.8、15.3和21.1,±0.2°2-θ。
在一些实施方案中,普拉克索的双羟萘酸盐的形式2可以通过具有以下峰中的一个或多个(例如,1、2、3、4、5、6、7或8)峰的xrpd谱表征:12.0、15.0、17.2、20.4、20.9、22.5、23.3和25.4,±0.2°2-θ。在一些实施方案中,普拉克索的双羟萘酸盐的形式2可以通过具有以下峰中的一个或多个(例如,1、2、3、4、5或6)峰的xrpd谱表征:12.0、15.0、20.4、20.9、22.5和23.3,±0.2°2-θ。在一些实施方案中,普拉克索的双羟萘酸盐的形式2可以通过具有以下峰中的一个或多个(例如,1、2、3或4)峰的xrpd谱表征:12.0、15.0、20.4和20.9,±0.2°2-θ。
在一些实施方案中,普拉克索的双羟萘酸盐的形式3可以通过具有以下峰中的一个或多个(例如,1、2、3、4、5、6、7或8)峰的xrpd谱表征:10.7、12.7、13.5、14.9、16.3、18.1、18.7和22.3,±0.2°2-θ。在一些实施方案中,普拉克索的双羟萘酸盐的形式3可以通过具有以下峰中的一个或多个(例如,1、2、3、4、5或6)峰的xrpd谱表征:10.7、12.7、13.5、14.9、18.7和22.3,±0.2°2-θ。在一些实施方案中,普拉克索的双羟萘酸盐的形式3可以通过具有以下峰中的一个或多个(例如,1、2、3或4)峰的xrpd谱表征:10.7、12.7、13.5和14.9,±0.2°2-θ。
在一些实施方案中,普拉克索的双羟萘酸盐的形式4可以通过具有以下峰中的一个或多个(例如,1、2、3、4、5、6、7、8、9或10)峰的xrpd谱表征:6.1、13.5、14.9、17.9、18.9、21.3、21.8、22.4、23.2和24.0,±0.2°2-θ。在一些实施方案中,普拉克索的双羟萘酸盐的形式4可以通过具有以下峰中的一个或多个(例如,1、2、3、4、5或6)峰的xrpd谱表征:6.1、17.9、18.9、21.3、23.2和24.0,±0.2°2-θ。在一些实施方案中,普拉克索的双羟萘酸盐的形式4可以通过具有以下峰中的一个或多个(例如,1、2、3或4)峰的xrpd谱表征:6.1、17.9、21.3和23.2,±0.2°2-θ。在一些实施方案中,普拉克索的双羟萘酸盐的形式4可以通过具有以下峰的xrpd谱表征:6.1和17.9,±0.2°2-θ。
在一些实施方案中,普拉克索的双羟萘酸盐的形式1至形式4中的每一种可以是基本上纯的,例如,每种形式可以基本上不含普拉克索双羟萘酸盐的其它结晶或无定形形式(例如,少于20%、少于10%、少于5%或用本文所述的xrpd方法检测不到)。然而,在一些实施方案中,普拉克索双羟萘酸盐的形式1至形式4的每一种可以与普拉克索双羟萘酸盐的一种或多种其它结晶或无定形的形式混合存在。
在一些实施方案中,本发明还提供了一种药物组合物,其包含一种或多种单胺抗pd药物的双羟萘酸盐(例如本文所述的任何一种,例如罗匹尼罗的双羟萘酸盐的晶型a-e、罗替戈汀的双羟萘酸盐的晶型i、普拉克索的双羟萘酸盐的晶型1-4)和至少一种药学上可接受的载体。在一些实施方案中,药物组合物是肌内或皮下注射制剂。在一个优选的实施方案中,药物组合物是包含单胺药物的双羟萘酸盐和聚合物(例如控释聚合物)的缓释制剂。适用于缓释制剂的聚合物包括本领域已知的任何聚合物。其中一些可以在例如remington'spharmaceuticalsciences,最新版本,mackpublishingco.中找到。在一些实施方案中,缓释可以基于本文双羟萘酸盐的缓慢的溶出速率。在一些实施方案中,缓释制剂还可以不含或基本上不含聚合物,例如,缓释制剂可以不含或基本上不含控制释放的聚合物。
在另一个实施方案中,药学上可接受的载体是粘性水性或非水性流体。在一些实施方案中,粘性的水性或非水性流体在20℃可以具有至少20cp的粘度。在一些实施方案中,粘性水性或非水性流体在20℃可以具有至少约30cp的粘度,例如,约40cp、约50cp、约60cp、至少约40cp、至少约50cp或至少约60cp。在一个优选的实施方案中,药物组合物在至少约24小时或至少约48小时的时间内释放有效量的活性剂(一种或多种本文所述的单胺药物的双羟萘酸盐)。在另一个优选的实施方案中,药物组合物中的活性剂具有至少约7天或至少约14天的功效持续时间。
本发明还涉及治疗患有与帕金森病相关的综合征的受试者的方法,诸如温血哺乳动物(如人类患者或特征为患有帕金森病的受试者)。所述方法包括施用治疗有效量的包含单胺药物的双羟萘酸盐(例如本文所述的任一种)和至少一种药学上可接受的载体的药物组合物。
在多个实施方案中,本发明人发现使用双羟萘酸作为抗衡离子形成的单胺药物的药学上可接受的盐,令人惊奇地具有非常低的溶解度(ksp)。当用于药物组合物中以提供单胺类药物的双羟萘酸盐的延长释放时,例如当肌内或皮下施用时,这种低溶解度是高度期望的。在一些实施方案中,本发明的药物组合物包括各种药物剂型,其目的是用于向需要治疗帕金森病的受试者(例如温血哺乳动物,例如人)施用剂量。在一些实施方案中,为了制备本发明的药物组合物,将药学有效量的一种或多种单胺药物的双羟萘酸盐(作为活性成分或活性剂)与一种或多种药学上可接受的赋形剂混合。所用的药学上可接受的赋形剂通常不太关键,是本领域公知的,并且可以根据施用所需的制剂形式采取多种形式。在一些实施方案中,这些药物组合物以适于施用的单位剂型提供。
本发明组合物的施用可以是例如胃肠外施用,例如通过皮下或肌内注射或植入。对于施用,单胺药物的双羟萘酸盐可以例如混悬在水性溶剂中,其可以进一步包含润湿剂,例如脱水山梨糖醇酯的聚氧乙烯衍生物,例如聚山梨酯80(
鉴于单胺药物的双羟萘酸盐在治疗帕金森病中的用途,在一些实施方案中,本发明还提供了治疗患有pd的温血哺乳动物(例如人)的方法。在一些实施方案中,该方法包括施用治疗有效量的药物组合物,其包含至少一种本文所述单胺药物的双羟萘酸盐和一种或多种药学上可接受的赋形剂。
在一些实施方案中,本文所述的药物组合物可以作为长效组合物施用于需要治疗帕金森病的受试者。在一个实施方案中,活性剂在至少约24小时,优选至少约48小时的时间内从组合物中释放。活性剂还可以以缓释组合物的形式施用。在一个实施方案中,缓释组合物在至少约7天,优选至少约14天,或者至少2周、至少3周、至少4周、至少6周或至少8周的时间内释放活性剂。该组合物可通过注射如肌内或皮下施用。在一个实施方案中,组合物可以作为单一或唯一剂量施用。然而,在一些实施方案中,本文所述的组合物对于需要持续或长期治疗的帕金森病的那些受试者,例如在数周或数月或更长时间内接受重复剂量的那些受试者特别有益。在这样的施用方案中,所述方法可以包括:(1)施用作为第一个剂量的含有一种或多种本文所述单胺药物的双羟萘酸盐的第一缓释组合物,然后(2)使用作为第二剂量的(以及,如需要,作为后续剂量的)第二缓释组合物。所述第二缓释组合物可以与第一缓释组合物相同、基本上相同或不同。具体地,在一些实施方案中,第二缓释组合物可以包括作为活性剂的一种或多种本文所述单胺药物的双羟萘酸盐,或者包括不同于本文所述单胺药物的双羟萘酸盐的活性剂。第二缓释组合物可以在第一次施用第一缓释组合物后约7天或更长时间,如至少约14天或至少约21天施用,其中第一次施用导致活性剂释放1天、2天、3天、4天、5天、6天、7天、8天、9天、10天、11天、12天、13天、14天或更长时间。
本文所用的、修饰本发明有关的量的术语“约”是指数量的变化,其可例如通过以下情况而发生:通过常规测试和处理;通过在所述测试和处理中的无意错误;通过本发明中所用成分的制造、来源或纯度的差异;等等。如本文所用,“约”特定值也包括该特定值,例如,约10%包括10%。无论是否用术语“约”修饰,权利要求包括所引用数量的等同方案。在一个实施方案中,术语“约”是指在所报告数值的20%内。
本文所用的术语“个体”、“受试者”或“患者”是指患有特定疾病状态的温血动物。温血动物包括哺乳动物,如人。
术语“有效量”或“治疗有效量”定义为导致任何参数或临床症状改善的量。在所述的任何实施方案中,术语“有效量”或“治疗有效量”可以是导致与帕金森病相关的任何参数或临床症状改善的量。实际剂量可以随每个患者而变化,并且并不是一定表示所有疾病症状的完全消除。本领域技术人员如主治医师,通过观察在类似情况下获得的结果和通过使用常规技术,可以容易地确定用于本文所述方法的化合物的治疗有效量。在确定治疗有效剂量时,主治医师考虑许多因素,包括但不限于:哺乳动物的物种;其大小、年龄和一般健康状况;所涉及的具体疾病;疾病的受累程度或严重性;个体患者的反应;所施用的特定化合物;施用方式;所施用制剂的生物利用度特征;选择的给药方案;伴随药物的使用;以及其他相关情况。
类似地,术语单胺在给定时间内的“功效持续时间”或“治疗有效血浆浓度”应理解为使得在该时间内,各单胺以足以导致任何参数或临床症状改善(例如与帕金森病相关的任何参数或临床症状改善)的量和/或浓度存在(例如在用本文双羟萘酸盐治疗的患者的血浆中)。
本领域技术人员可以根据所选化合物的具体特征、待治疗的疾病状态、疾病阶段和其它相关情况,使用本领域已知的制剂技术容易地确定优选的施用量和施用方式,所述制剂技术描述于例如remington'spharmaceuticalsciences,最新版,mackpublishingco中。
药物组合物可以利用本领域已知的常规技术制备。通常,治疗有效量的化合物(盐)将与药学上可接受的载体组合。
本发明的药物组合物可以肠胃外施用。例如,它们可以通过注射施用。优选的肠胃外施用方法包括肌内和皮下注射。
对于肠胃外施用,化合物(盐)可以溶解在生理学上可接受的药物载体中,并作为溶液或混悬剂施用。优选粘性可注射载体,其在20℃具有例如至少20cp的粘度。在其它实施方案中,混悬剂的流体相在20℃下具有至少约30cp的粘度,例如约40cp、约50cp、约60cp、至少约40cp、至少约50cp或至少约60cp。该组合物还可包含粘度增强剂、密度增强剂、张力增强剂和/或润湿剂。合适的药物载体包括水、盐水、右旋糖溶液、果糖溶液、乙醇或者动物、植物或合成来源的油。药物载体还可以含有如本领域已知的防腐剂和缓冲剂。
当组合物用作可注射材料时,包括但不限于无针注射,其可以配制到常规的可注射载体中。合适的载体包括生物相容的和药学上可接受的溶液、乳液或混悬液。
在另一个实施方案中,制剂可以通过外科手术植入。这样的制剂可以包括任何公知的可生物降解和可生物溶蚀的载体,例如聚交酯、聚-丙交酯-共-乙交酯和胶原制剂。这种材料可以是固体植入物、海绵等形式。在任何情况下,对于材料的局部使用,活性成分通常以约1:1000至1:20,000的重量比存在于载体或赋形剂中,但不限于在该范围内的比例。
在一些实施方案中,本发明还提供了制备单胺药物的双羟萘酸盐的方法。具体地,单胺药物的双羟萘酸盐可以以多种不同的方式制备。例如,在一个实施方案中,单胺药物的双羟萘酸盐可通过在溶剂(例如水、乙醇或dmso)中,用双羟萘酸处理单胺药物(例如游离碱)或与单胺药物(例如游离碱)混合而直接制备。在另一个实施方案中,单胺药物的双羟萘酸盐可以通过在一种或多种溶剂中,用双羟萘酸盐(例如双羟萘酸二钠)处理单胺药物盐(例如盐酸盐)或与单胺药物盐(例如盐酸盐)混合来制备。例如,可通过将双羟萘酸二钠或其它双羟萘酸盐在适当溶剂如水中的溶液加入单胺药物盐酸盐的溶液中,并将该溶液搅拌一段时间,如约3或12小时,直至发生沉淀,来制备单胺药物的双羟萘酸盐。或者,也可以使用其它方法如蒸发、浆化、反溶剂、冷却和水合来使盐结晶。可用于制备本文双羟萘酸盐的溶剂包括但不限于水、链烷醇(例如甲醇和乙醇)、烷基酮(例如丙酮)、烷烃(例如正庚烷)、乙腈、甲苯、dmso、烷基酯(例如乙酸乙酯)、卤代烷烃(例如氯仿)、醚、四氢呋喃(thf)、1,4-二噁烷及其组合。
在一些实施方案中,本发明提供多巴胺激动剂罗替戈汀、罗匹尼罗和普拉克索的药学上可接受的盐的固态形式,其中所述盐是双羟萘酸盐。双羟萘酸盐可以是结晶的、无水的、水合的、溶剂化的或无定形的。在另一个实施方案中,本发明涉及结晶的罗替戈汀、罗匹尼罗或普拉克索的双羟萘酸盐,其具有或特征在于一种或多种以下性质:(1)对于每种晶型,分别与图1、3、5、7、9、11、13、15、17、19所示的那些基本上一致的x-射线粉末衍射图;(2)对于每种晶形,分别与图2、4、6、8、10、12、14、16、18、20中所示的那些基本上一致的差示扫描量热法热分析图;和(3)(1)和(2)的组合。在一些实施方案中,本发明还涉及含有一种或多种上述罗替戈汀、罗匹尼罗和普拉克索的双羟萘酸盐的组合物,以及含有所述组合物和至少一种药学可接受载体的药物组合物。
在一些实施方案中,本发明提供了抗pdmao-b抑制剂司来吉兰、雷沙吉兰和沙芬酰胺的药学上可接受的盐的固态形式,其中所述盐为双羟萘酸盐。双羟萘酸盐可以是结晶的、无水的、水合的、溶剂化的或无定形的。在一些实施方案中,本发明还提供了含有一种或多种上述司来吉兰、雷沙吉兰和沙芬酰胺的双羟萘酸盐的组合物,以及含有所述组合物和至少一种药学上可接受的载体的药物组合物。
以下实施例旨在说明而不是限制本发明的范围。
实施例
实施例1
从dmso和水的混合物中制备罗匹尼罗与双羟萘酸摩尔比为1:1的罗匹尼罗双羟萘酸盐。
在搅拌下将罗匹尼罗(2g,7.7mmol)和双羟萘酸(2.975g,7.7mmol)加入dmso(15ml)中以形成溶液。在室温将得到的溶液缓慢加入水(500ml)中,产生白色固体。在过滤器上收集固体,用水洗涤,并在40℃真空下干燥,生成罗匹尼罗的双羟萘酸盐,为白色固体(4.0g,80.4%)。
使用brukerd8advancex-射线粉末衍射仪,用铜kα辐射在1.54nm波长,获得上述固体的x-射线粉末衍射(“xrpd”)图。仪器条件包括每步0.02度的步长、每步0.2秒的扫描速率、3至40度的2θ范围、40kv的电压、40ma的电流和lynxye检测器。将样品装入凹陷的样品架中进行分析。通常,2θ值的误差容限为±0.2°。类似地获得了本文其它实施例的xrpd图。实施例1的盐的x-射线粉末衍射图和数据的典型实例分别示于图1和表1中,其中d(a)表示晶面间距。高度和h%代表典型的相对强度。
上述固体的差示扫描量热法热分析图是使用tainstrumentq200差示扫描量热计获得的。通过“thermaladvantage”系统控制测量,并使用“universalanalysis”软件分析数据。典型的样品载量范围为0.5至5mg。在氮气气氛下以40ml/min的流速进行测量。将系统平衡设定在20℃,然后以10℃/分钟的速率将温度升高至250℃。通常,dsc峰值的误差范围是±3℃,类似地获得了本文其它实施例的dsc热分析图。实施例1的盐的差示扫描量热法热分析图的典型实例示于图2中。1hnmr(见图23)表明实施例1的盐中罗匹尼罗与双羟萘酸的摩尔比为约1:1。
表1
实施例2
通过将图1和2所示的批料在170℃加热30分钟制备罗匹尼罗与双羟萘酸摩尔比1:1的罗匹尼罗双羟萘酸盐
将75mg实施例1的罗匹尼罗的双羟萘酸盐在170℃放置30分钟,得到固体,其x-射线衍射图的典型实例如图3和表2所示。该固体的差示扫描量热法热分析图的典型实例示于图4中。1hnmr表明该固体中罗匹尼罗与双羟萘酸的摩尔比为约1:1。
表2
实施例3
从乙醇、水和peg6000的混合物中制备罗匹尼罗与双羟萘酸摩尔比为2:1的罗匹尼罗双羟萘酸盐。
在室温下将100mg实施例1的罗匹尼罗的双羟萘酸盐溶于14ml乙醇和7ml水的混合物中。向溶液中加入10%peg6000,并通过超声溶解得到的混合物,然后将其在40℃浓缩,得到固体。然后收集该固体,洗涤并干燥。该固体的x-射线衍射图的典型实例示于图5和表3中。该固体的差示扫描量热法热分析图的典型实例示于图6中。1hnmr(见图24)表明实施例3的盐中罗匹尼罗与双羟萘酸的摩尔比为约2:1。
表3
实施例4
从dmso和乙腈的混合物中制备罗匹尼罗与双羟萘酸摩尔比为1:1的罗匹尼罗双羟萘酸盐。
将100mg实施例1的罗匹尼罗的双羟萘酸盐溶解在0.45ml二甲亚砜(dmso)中。在室温向该溶液中加入5ml乙腈。然后将所得溶液在4℃搅拌以产生固体,将其收集、洗涤并干燥。该固体的x-射线衍射图的典型实例示于图7和表4中。该固体的差示扫描量热法热分析图的典型实例示于图8中。1hnmr表明该固体中罗匹尼罗与双羟萘酸的摩尔比为约1:1。
表4
实施例5
从乙醇、水和聚(烯丙胺盐酸盐)的混合物中制备罗匹尼罗与双羟萘酸摩尔比为2:1的罗匹尼罗的双羟萘酸盐。
将100mg实施例1的罗匹尼罗的双羟萘酸盐溶解在14ml乙醇和7ml水的混合物中。向该溶液中加入10%聚(烯丙胺盐酸盐)。在40℃保持蒸发后,形成固体,并通过xrpd和dsc表征。该固体的x-射线衍射图的典型实例示于图9和表5中。该固体的差示扫描量热法热分析图的典型实例示于图10中。1hnmr表明该固体中罗匹尼罗与双羟萘酸的摩尔比为约2:1。
表5
实施例6
从乙醇、丙酮和正庚烷的混合物中制备罗替戈汀与双羟萘酸摩尔比为1:1的罗替戈汀双羟萘酸盐。
通过超声处理将35.2mg罗替戈汀盐酸盐溶于4ml丙酮和1ml乙醇的混合物中。另外,将41mg双羟萘酸钠溶解在2ml乙醇和0.4ml丙酮的混合物中。向罗替戈汀盐酸盐溶液中滴加双羟萘酸钠溶液。加入并搅拌30分钟后,加入4ml正庚烷,将所得溶液搅拌过夜,生成罗替戈汀双羟萘酸盐结晶固体。收集固体,用水洗涤,真空干燥,并通过xrpd和dsc表征。该固体的x-射线衍射图的典型实例示于图11和表6中。该固体的差示扫描量热法热分析图的典型实例示于图12中。1hnmr(参见图25)表明该固体中罗替戈汀与双羟萘酸的摩尔比为约1:1。
表6
实施例7
从丙酮和水的混合物制备普拉克索与双羟萘酸摩尔比为1:1的普拉克索双羟萘酸盐。
在室温下,通过搅拌将普拉克索(3.0g,14.1mmol)和双羟萘酸(2.7g,7.0mmol)溶解在dmso(30ml)中。然后在室温下将该溶液缓慢加入到乙酸乙酯(2l)中,产生白色固体。在过滤器上收集固体,并在45℃真空干燥,得到普拉克索与双羟萘酸的摩尔比为2:1的无定形普拉克索双羟萘酸盐(4.5g,78.6%)。
在60℃将100mg上述无定形普拉克索双羟萘酸盐溶于3ml丙酮和0.5ml水的混合物中。将该溶液缓慢冷却至室温,并搅拌3小时,得到固体形式的普拉克索双羟萘酸盐,将其收集、洗涤并干燥。通过xrpd和dsc表征该固体。该固体的x-射线衍射图的典型实例示于图13和表7中。该固体的差示扫描量热法热分析图的典型实例示于图14中,1hnmr(参见图21)表明在该固体中普拉克索与双羟萘酸的摩尔比为约1:1。
表7
实施例8
从丙酮和甲醇的混合物中制备普拉克索与双羟萘酸摩尔比为1:1的普拉克索双羟萘酸盐。
在室温将100mg实施例7的无定形普拉克索双羟萘酸盐溶于0.6ml甲醇中。在搅拌下向该溶液中加入3ml丙酮,得到结晶固体状的普拉克索双羟萘酸盐,将其收集、洗涤并干燥。通过xrpd和dsc表征该固体。该固体的x-射线衍射图的典型实例示于图15和表8中。该固体的差示扫描量热法热分析图的典型实例示于图16中。1hnmr表明在该固体中普拉克索与双羟萘酸的摩尔比为约1:1。
表8
实施例9
从乙酸乙酯溶液中制备普拉克索与双羟萘酸摩尔比为2:1的普拉克索双羟萘酸盐。
将50mg实施例7的无定形普拉克索双羟萘酸盐溶于2.5ml乙酸乙酯中。将溶液在室温搅拌5天,得到普拉克索双羟萘酸盐,为固体,将其收集、洗涤并干燥。通过xrpd和dsc表征固体。该固体的x-射线衍射图的典型实例示于图17和表9中。该固体的差示扫描量热法热分析图的典型实例示于图18中。1hnmr(参见图26)表明在该固体中普拉克索与双羟萘酸的摩尔比为约2:1。
表9
实施例10
从四氢呋喃溶液中制备普拉克索与双羟萘酸摩尔比为2:1的普拉克索双羟萘酸盐
将50mg实施例7的无定形普拉克索双羟萘酸盐溶于2.5ml四氢呋喃(thf)中。将溶液在室温搅拌10天,得到普拉克索双羟萘酸盐,其为固体,将其收集、洗涤并干燥。通过xrpd和dsc表征固体。该固体的x-射线衍射图的典型实例示于图19和表10中。该固体的差示扫描量热法热分析图的典型实例示于图20。1hnmr(见图22)表明在该固体中普拉克索与双羟萘酸的摩尔比为约2:1。
表10
实施例11
通过质子核磁共振谱(1h-nmr)表征普拉克索与双羟萘酸摩尔比为1:1或2:1的普拉克索双羟萘酸盐。
使用1h-nmr分析普拉克索双羟萘酸盐(1:1和2:1)。1h-nmr谱提供于图21和22中。图21是从丙酮和水的混合物制备的1:1盐(实施例7)的1h-nmr谱。由1hnmr谱的质子积分测量的普拉克索与双羟萘酸的摩尔比为约1:1。1hnmr(500mhz,dmso-d6)化学位移记录在(所有值以ppm计)8.65(b,2h),8.28(s,2h),8.17(d,2h),7.73(d,2h),7.21(t,2h),7.09(t,2h),6.84(s,2h),4.72(s,2h),3.49(m,3h),2.97(m,3h),2.50-2.68(m,6h),2.17(m,1h),1.83(m,1h),1.65(m,2h),0.94(t,3h)。图22是在四氢呋喃溶液中制备的2:1盐(实施例10)的1h-nmr谱。由1h-nmr谱的质子积分测得普拉克索与双羟萘酸的摩尔比约为2:1。1h-nmr(500mhz,dmso-d6)化学位移记录在(inppm)8.65(b,2h),8.19(m,2h),7.63(d,1h),7.11(m,1h),6.99(m,1h),6.78(s,2h),4.67(s,1h),3.59(m,2h),3.49(m,1h),2.97(m,3h),2.50-2.68(m,3h),2.17(m,1h),1.51-1.83(m,5h),1.65(m,2h),0.95(t,3h)。
实施例12
使用不同溶剂系统的普拉克索双羟萘酸盐的晶形筛选。
本实施例提供了上述实施例中描述的普拉克索双羟萘酸盐的晶形筛选总结。用于制备普拉克索双羟萘酸盐的晶形的溶剂是重要的,因为许多溶剂或溶剂系统不能用于形成结晶盐形式。
筛选了一系列溶剂或这些溶剂的组合,包括水、链烷醇(例如甲醇和乙醇)、烷基酮(例如丙酮)、烷烃(例如正庚烷)、乙腈、甲苯、dmso、烷基酯(例如乙酸乙酯)、卤代烷烃(例如氯仿)、thf和1,4-二噁烷,以产生普拉克索双羟萘酸盐的晶形。使用这些溶剂,使用本领域技术人员已知的不同类型的结晶技术(包括冷却、蒸发和加入第二溶剂)以降低溶质的溶解度(称为抗溶剂或赶出(drown-out)的技术)。
当丙酮和水的混合物或丙酮和甲醇的混合物用作溶剂系统时,使用无定形普拉克索双羟萘酸盐得到两种不同的单普拉克索双羟萘酸盐晶型,如实施例7和8所述。然而,如实施例9和10所述,当使用乙酸乙酯或四氢呋喃(thf)作为溶剂系统时,由无定形普拉克索双羟萘酸盐获得两种不同的半普拉克索双羟萘酸盐晶形。
在使用上述溶剂系统获得的单普拉克索双羟萘酸盐的两种晶形之间,实施例7中由丙酮和水获得的晶形更稳定。在室温静置7天后,实施例8的晶形开始转化为实施例7中所述的晶形。对于半普拉克索双羟萘酸盐的两种晶形,实施例10中描述的形式更稳定。当在室温下置于干燥箱中时,实施例9的半普拉克索双羟萘酸盐的晶形转化为无定形态。
实施例13
从dmso和水的混合物中制备罗匹尼罗与双羟萘酸摩尔比为2:1的罗匹尼罗双羟萘酸盐。
搅拌下将罗匹尼罗(1.3g,5mmol)和双羟萘酸(0.967g,2.5mmol)加入到dmso(8ml)中形成溶液。在室温下将所得溶液缓慢加入到水(250ml)中,产生白色固体。在过滤器上收集固体,用水洗涤,并在45℃真空干燥,得到罗匹尼罗双羟萘酸盐,为白色固体(2.1g,92.6%)。
实施例14
a.从dmso和水的混合物中制备罗替戈汀与双羟萘酸摩尔比为1:1的罗替戈汀双羟萘酸盐。
在搅拌下将罗替戈汀(3g,9.51mmol)和双羟萘酸(3.68g,9.51mmol)加入dmso(40ml)中形成溶液。在室温将所得溶液缓慢加入到水(500ml)中,得到白色固体。在过滤器上收集固体,用水洗涤,并在45℃真空干燥,得到罗替戈汀双羟萘酸盐,为白色固体(5g,74.9%)。
b.从dmso和水的混合物中制备罗替戈汀与双羟萘酸摩尔比为2:1的罗替戈汀双羟萘酸盐。
在搅拌下将罗替戈汀(1g,3.17mmol)和双羟萘酸(0.614g,1.585mmol)加入dmso(8ml)中形成溶液。在室温将所得溶液缓慢加入到水(500ml)中,得到白色固体。在过滤器上收集固体,用水洗涤,并在45℃真空干燥,得到罗替戈汀双羟萘酸盐,为白色固体(2g,77.4%)。
实施例15
从dmso和乙酸乙酯(ea)的混合物制备普拉克索与双羟萘酸摩尔比为1:1的普拉克索双羟萘酸盐。
在室温通过搅拌将普拉克索(5.0g,23.44mmol)和双羟萘酸(9.08g,23.44mmol)溶解在dmso(50ml)中。然后在室温将该溶液缓慢加入到乙酸乙酯(2l)中,产生白色固体。在过滤器上收集固体,并在45℃真空干燥,得到普拉克索与双羟萘酸摩尔比为1:1的普拉克索双羟萘酸盐(14.0g,99.0%)。
应当理解,详述部分,而非发明概述和摘要部分,旨在用于解释权利要求。概述和摘要部分可以阐述发明人所预期的本发明的一个或多个但不是所有的示例性实施方案,因此,不意欲以任何方式限制本发明和所附权利要求。
上文已经借助于功能构建块描述了本发明,所述模块示出了特定功能及其关系的实现。为了便于描述,在此已经任意定义了这些功能性构建块的边界。只要适当地实施所述特定的功能及其关系,就可以定义用作替换的边界。
就本发明描述为一类事物的方面而言,所有单个事物各自被认为是本发明的单独方面。如果本发明的方面被描述为"包括"特征,则实施方案也涉及"由该特征组成"或"基本上由该特征组成"。
上述具体实施方案的描述将如此充分地揭示本发明的一般性质,以使其他人可以通过应用本领域技术人员的知识,在不偏离本发明的一般概念的情况下,在不进行过度实验的情况下,容易地修改和/或调整这些具体实施方案以用于各种应用。因此,基于本文所呈现的教导和指导,此类调整和修改旨在处于所公开的实施例的等同方案的含义和范围内。应当理解,本文的措辞或术语是为了描述而不是限制的目的,使得本说明书的术语或措辞将由技术人员根据所述教导和指导来解释。
本发明的广度和范围不应由任何上述示例性实施方案限制,而应仅根据所附权利要求及其等同方案来限定。
本文描述的所有各个方面、实施方案和选项可以以任何和所有变化形式组合。
本说明书中提及的所有出版物、专利和专利申请均并入本文作为参考,其程度如同每个单独的出版物、专利或专利申请被具体地和单独地指明并入本文作为参考。当本发明中术语的任何含义或定义与引入以供参考的文件中术语的任何含义或定义矛盾时,应当以在本发明中赋予该术语的含义或定义为准。
- 还没有人留言评论。精彩留言会获得点赞!