用于将微针阵列施用于皮肤的施用装置的利记博彩app
相关申请的交叉引用
本申请要求2017年10月17日提交的美国临时专利申请62/573,513和2017年11月22日提交的美国临时专利申请62/589,717的权益,这些美国临时专利申请的公开内容全文以引用方式并入本文中。
本公开整体涉及用于将微针装置施用于皮肤以处理皮肤区域和/或将活性剂递送至患者的施用装置和方法。
背景技术:
透皮和局部药物递送可用于治疗处理,但可使用这些路线有效递送的分子数可通过皮肤的阻隔性进行限制。分子通过皮肤传送的主要障碍是角质层(皮肤的最外层)。
已提出了多种不同的皮肤处理方法,以便提高诸如角质层等最外皮肤层的渗透性或孔隙率,从而增强通过那些层或至那些层中的递送。角质层为由脂域分开的紧凑角化的细胞残余物的复杂结构。角质层是由失去其细胞核并且变为角质的角质细胞形成的,该角质细胞包括大多数上皮细胞。这些死细胞构成角质层,该角质层具有仅约10-30微米的厚度并且防止身体被外源性物质侵入并防止内源性流体和溶解分子向外迁移。各种皮肤处理方法包括使用微针、激光消融、射频消融、热消融、超声波导入、离子导入、或这些处理方法的组合。
已公开了包括相对较小结构(有时称为微针或微钉)的阵列的装置以结合治疗剂和其他物质通过皮肤和其他表面的递送来使用。可将装置压贴皮肤以努力刺穿角质层,使得治疗剂和其他物质可以顺序或同时穿过该层并进入下面的组织中。这些装置的微针会在接触角质层时将其刺穿,从而形成多个微观狭缝,微观狭缝用作通道,活性组分的分子可以通过通道被递送到主体内。为了递送活性组分,微针装置可以设置有贮存器,用于在将活性组分递送穿过角质层之前暂时地保持液态形式的活性组分。在一些构造中,微针可以为空心的,以提供直接从贮存器通过微针的液体流动路径,以使得能够穿过皮肤递送治疗物质。在替代构造中,可以将活性组分涂布在微针阵列上,并在已刺穿角质层之后将活性组分直接穿过皮肤递送。
微针阵列和贴片可与能够多次使用的施用装置一起进行部署。微针阵列和贴片通常使用一次,并且然后丢弃。施用装置可重复地重新加载新的微针阵列和贴片。本公开描述了微针阵列施用装置。
技术实现要素:
本公开涉及可用于处理所选择位点(例如,在皮肤上)和/或将活性成分施用于处理位点的施用装置。各种实施方案包括但不限于下列结构:
1.一种用于将微针阵列施用于表面的装置,所述装置包括:
主体,所述主体包括限定腔体的第一部分和第二部分,所述第二部分包括存在于所述第二部分的外表面上的用于将所述微针阵列插入所述腔体中的狭槽,所述第一部分和所述第二部分能够沿轴线相对于彼此滑动,使得所述主体处于未装填构型和装填构型;和
门,所述门能够与所述第二部分一起操作,所述门能够从第一门位置移动到第二门位置,
其中当所述装置处于所述未装填构型时,所述门处于所述第一门位置并且至少部分地阻塞所述狭槽和通向所述腔体的通道,并且
其中当所述装置处于所述装填构型时,所述门处于所述第二门位置并且不阻塞所述狭槽以实现通向所述腔体的通道。
2.根据实施方案1所述的装置,还包括微针阵列。
3.根据实施方案2所述的装置,其中所述微针阵列包括多个微针。
4.根据实施方案1所述的装置,还包括邻近所述狭槽的着色视觉标记或其他视觉标记,从而向使用者标识所述狭槽的位置。
5.根据实施方案1所述的装置,还包括在所述门上呈现着色视觉标记或其他视觉标记,使得当所述门处于所述第一门位置时,使用者知道所述门至少部分地阻塞通向所述腔体的通道。
6.根据实施方案1所述的装置,还包括偏置构件,所述偏置构件用于在处于所述未装填构型时使所述门偏置到所述第一位置。
7.根据实施方案5所述的装置,其中所述偏置构件包括压缩弹簧。
8.根据实施方案1所述的装置,还包括设置在所述腔体中的柱塞,所述柱塞包括第一柱塞端部和第二柱塞端部,所述柱塞能够从所述装置处于所述未装填构型时的第一柱塞位置移动到所述装置处于所述装填构型时的第二柱塞位置,其中当所述柱塞移动到所述第二柱塞位置时,所述第二柱塞端部与所述门可操作地接合以使所述门移动到所述第二门位置。
9.根据实施方案8所述的装置,还包括偏置构件,所述偏置构件用于在所述主体处于所述未装填构型时使所述柱塞偏置到所述第一柱塞位置。
10.根据实施方案9所述的装置,其中所述偏置构件包括压缩弹簧。
11.根据实施方案10所述的装置,其中当所述柱塞处于在所述主体处于所述装填构型时的所述第二柱塞位置时,所述压缩弹簧被压缩和供能。
12.一种用于将微针阵列施用于表面的装置,所述装置包括:
主体,所述主体包括限定腔体的第一部分和第二部分,所述第二部分包括存在于所述第二部分的外表面上的用于将所述微针阵列插入所述腔体中的狭槽,所述第一部分和所述第二部分能够沿轴线相对于彼此滑动,因此使得所述主体处于未装填构型和装填构型;和
柱塞,所述柱塞设置在所述腔体中,所述柱塞包括第一柱塞端部和第二柱塞端部,所述柱塞能够从所述装置处于所述未装填构型时的第一位置移动到所述装置处于所述装填构型时的第二位置,
其中当所述装置处于所述装填构型时,微针阵列能够穿过所述狭槽插入所述腔体中并定位成使得其邻近所述第二柱塞端部。
13.根据实施方案12所述的装置,还包括微针阵列。
14.根据实施方案12所述的装置,其中微针阵列插入所述狭槽中并且邻近所述第二柱塞端部定位,所述微针阵列和所述第二柱塞端部彼此接触。
15.根据实施方案12所述的装置,其中微针阵列插入所述狭槽中并且邻近所述第二柱塞端部定位,所述微针阵列和所述第二柱塞端部彼此相距小于约2mm。
16.根据实施方案12所述的装置,其中微针阵列插入所述狭槽中并且邻近所述第二柱塞端部定位,所述微针阵列和所述第二柱塞端部彼此相距小于约1mm。
17.根据实施方案12所述的装置,其中微针阵列插入所述狭槽中并且邻近所述第二柱塞端部定位,所述微针阵列和所述第二柱塞端部彼此相距小于约0.5mm。
18.根据实施方案12所述的装置,其中所述第二部分包括内表面,所述内表面包括低表面能材料,其中当所述柱塞从所述第一位置移动到所述第二位置时,如果微针阵列和所述内表面彼此可滑动地接合,则它们之间的任何摩擦最小化。
19.根据实施方案12所述的装置,还包括偏置构件,所述偏置构件用于在所述主体处于所述未装填构型时使所述柱塞偏置到所述第一柱塞位置。
20.根据实施方案19所述的装置,其中所述偏置构件包括压缩弹簧。
21.根据实施方案20所述的装置,其中当所述柱塞处于在所述主体处于所述装填构型时的所述第二柱塞位置时,所述压缩弹簧被压缩和供能。
22.一种与微针阵列施用装置一起使用的插入件,所述插入件包括限定腔体的外壳和存在于所述外壳中的能够在第一位置和第二位置之间移动的递送机构,所述插入件包括:
用于插入所述施用装置的腔体中的第一端部,以及与所述第一端部大致相反的第二端部;以及
从所述第一端部延伸至所述第二端部的边界结构,所述边界结构包括内表面和外表面,所述内表面限定开口,所述开口包括从所述内表面延伸到所述开口中的一个或多个突起部,
其中所述边界结构基本上但不完全包封所述开口,使得在邻近所述第一端部的所述边界结构中存在间隙。
23.一种与用于施用微针阵列的装置一起使用的插入件,所述插入件包括限定腔体的外壳和存在于所述外壳中的能够在第一位置和第二位置之间移动的递送机构,所述插入件包括:
用于插入所述施用装置的腔体中的第一端部,以及与所述第一端部大致相反的第二端部;以及
从所述第一端部延伸至所述第二端部的边界结构,所述边界结构包括内表面和外表面,所述内表面限定开口,所述开口包括从所述内表面延伸到所述开口中的一个或多个突起部,
其中所述一个或多个突起部由低表面能材料构成。
24.根据实施方案23所述的插入件,其中所述微针阵列包括在其一部分上的粘合剂,所述粘合剂粘附到包含所述低表面能材料的所述一个或多个突起部。
25.一种将微针阵列施用于皮肤的方法,所述方法包括:
提供用于施用的装置,所述装置包括:
主体,所述主体包括纵向轴线以及限定腔体的第一部分和第二部分,所述第二部分包括存在于所述第二部分的外表面上的用于将微针阵列插入所述腔体中的狭槽,所述第一部分和所述第二部分能够沿所述纵向轴线相对于彼此滑动,使得所述主体处于未装填构型和装填构型;
门,所述门能够与所述第二部分一起操作,所述门能够从第一门位置移动到第二门位置,
其中当所述装置处于所述未装填构型时,所述门处于所述第一门位置并且至少部分地阻塞所述狭槽和通向所述腔体的通道,并且
其中当所述装置处于所述装填构型时,所述门处于所述第二门位置并且不阻塞所述狭槽以实现通向所述腔体的通道;和
柱塞,所述柱塞包括第一端部和第二端部并且设置在所述腔体中,所述柱塞能够从所述装置处于所述未装填构型时的第一柱塞位置移动到所述装置处于所述装填构型时的第二柱塞位置,所述柱塞还包括柱子,所述柱子包括柱子宽度,
其中当所述装置处于所述装填构型时,微针阵列能够穿过所述狭槽插入所述腔体中并定位成使得其邻近所述柱塞的所述第二端部,并且
其中当所述装置处于所述装填构型时,与所述柱塞相关联的柱塞弹簧被压缩和供能;
轴向压缩所述第一部分和所述第二部分,使得所述第一部分和所述第二部分可操作地沿轴线相对于彼此可滑动地移动,使得装置能够从所述未装填构型移动到所述装填构型;
将所述微针阵列穿过所述狭槽插入所述腔体中,使得所述微针阵列邻近所述柱塞的所述第二端部定位;
轴向压缩所述第一部分和所述第二部分,从而导致释放所述柱塞,其中所述柱塞弹簧在供能时驱动所述微针阵列朝向患者的皮肤,使得其被递送至患者的皮肤。
26.根据实施方案25所述的方法,所述方法还包括:
提供插入件,所述插入件包括从所述第一端部延伸至所述第二端部的边界结构,所述边界结构包括内表面和外表面,所述内表面限定开口,所述开口包括从所述内表面延伸到所述开口中的一个或多个突起部,其中所述微针阵列包括在其一部分上的粘合剂,所述粘合剂粘附到包含所述低表面能材料的所述一个或多个突起部,使得所述微针阵列定位在开口中,
其中所述边界结构基本上但不完全包封所述开口,使得在邻近所述第一端部的所述边界结构中存在间隙,所述间隙的尺寸与所述柱子宽度大约相同或更大,
其中通过所述狭槽将所述微针阵列插入所述腔体中的所述步骤包括通过所述狭槽将所述插入件插入所述腔体中;以及
在所述微针阵列已到达所述患者的皮肤之后从所述腔体中移除所述插入件,其中在此类移除期间,所述间隙移动经过所述柱塞柱子,使得当柱塞处于所述第一柱塞位置时能够移除插入件。
27.一种用于将微针阵列施用于皮肤的套件,所述套件包括提供根据实施方案1-24中任一项所述的装置和根据实施方案25-26中任一项所述的方法的说明书。
在其中使用低表面能材料的实施方案中,此类材料可优选地包括小于约37mj/mm2、小于约29mj/mm2、或小于约18mj/mj/mm2的表面能。此类低表面能材料可包括,例如聚乙酸乙烯酯(pva)、聚丙烯(pp)和聚四氟乙烯(ptfe)。
参考具体实施方式和附图,本公开的其他特征和方面将变得显而易见。
附图说明
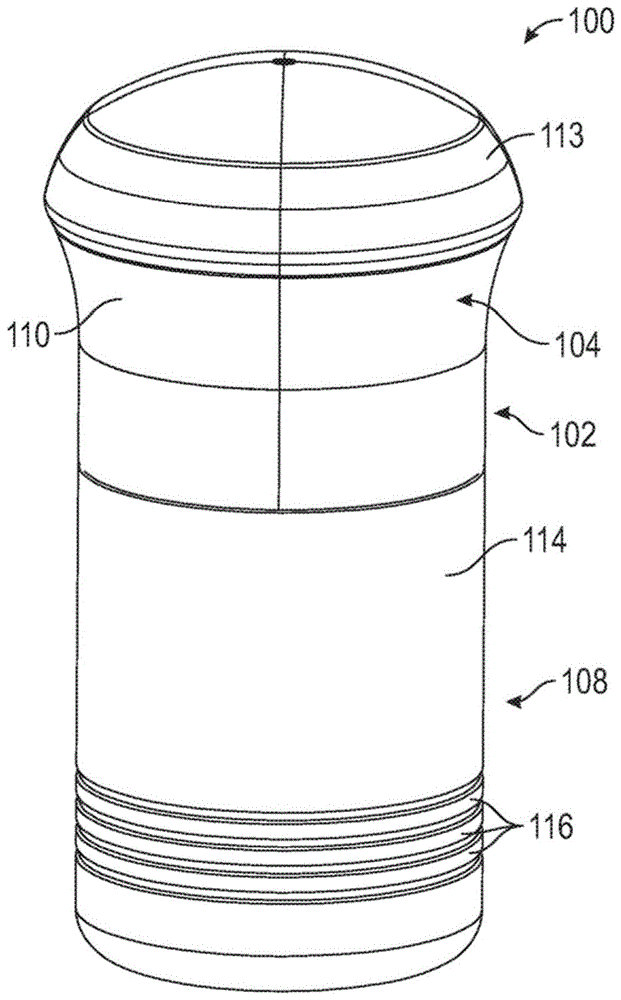
图1为根据本公开的实施方案的施用装置的顶部透视图。
图2为移除了覆盖件的图1的施用装置的透视图。
图3为图1和2的施用装置的前正视图。
图4为微针阵列载体的顶部透视图。
图5为图4的微针阵列载体的底部平面视图。
图6为具有微针阵列的图4和5的微针阵列载体的顶部透视图。
图7为图6的微针阵列载体的顶部平面图。
图8为图6的微针阵列载体的底部透视图。
图9为图6的微针阵列载体的底部平面视图。
图10为根据本公开的一个实施方案的微针装置的底部透视图。
图11为图10的微针装置的底部平面视图。
图12为图10的微针装置的顶部平面图。
图13为微针阵列的特写侧正视图(示出微针指向上)。
图14为根据本公开的一个实施方案的施用装置的顶部前透视图和局部剖视图。
图15为图14的施用装置的顶部前透视图和局部剖视图。
图16为图14的施用装置的顶部前透视图和局部剖视图。
图17为图14的施用装置和图6的微针阵列载体的顶部前透视图和局部剖视图。
图18为图14的施用装置和图6的微针阵列载体的顶部前透视图和局部剖视图。
图19为图14的施用装置和图6的微针阵列载体的顶部前透视图和局部剖视图。
图20为图14的施用装置和图6的微针阵列载体的顶部前透视图和局部剖视图。
图21-24为图14的施用装置和图6的微针阵列载体的特写局部剖视图。
图25为根据本公开的一个实施方案的施用装置的第一顶部平面图,其中移除了上部外壳的顶盖以示出闩锁和柱塞机构的上部部分。
图26为图25的施用装置的第二顶部平面图。
图27为图25的施用装置的第一部分切除视图,其中上部外壳的顶盖处于适当的位置。
图28为图27的施用装置的第二部分切除视图。
具体实施方式
在详细解释本公开的任何实施方案之前,应当理解,本发明在其应用中不限于下文说明中所提及或下文附图中所示出的构造细节和组件布置方式。本发明能够具有其他实施方案,并且能够以各种方式实践或实施。而且,应当理解,本文使用的措辞和术语是用于说明目的而不应视为限制性的。本文中“包括”、“包含”或“具有”及其变型的使用意指涵盖其后所列举的项目及其等同形式以及附加的项目。除非另有规定或限制,术语“联接”及其变型形式被广义地应用并涵盖直接联接和间接联接。此外,术语诸如“前部”、“后部”、“顶部”、“底部”、“向上”、“向下”、“在……下方”等仅用于在元件彼此相关时描述元件,但绝非意在描述装置的具体取向、指示或暗示装置的必要或需要的取向、或规定本文所述的发明在使用时将如何使用、安装、显示或定位。
在讨论本公开的施用装置时,有时使用术语“向下”及其变型形式来描述微针被按压到皮肤中的方向,并使用“向上”来描述相反的方向。然而,本领域的技术人员将理解,所述施用装置可在微针与地球引力的方向成一角度或甚至沿与地球引力的方向相反的方向按压到皮肤中的情况下使用,并且这些术语仅为简明和清晰起见而被用来描述相对方向。
术语“透皮”及其变型形式通常用于指代对穿越皮肤的任何部分的活性成分的任何类型的递送。即,透皮通常可包括全身递送(即,在活性成分穿过真皮或基本上通过真皮输送,使得活性成分递送到血流中的情况下)以及皮内递送(即,在活性成分部分地通过真皮(例如,穿过皮肤的外层(角质层))输送的情况下,在活性成分递送到皮肤中,例如用于治疗牛皮癣或用于局部麻醉剂递送的情况下)。即,如本文所用的透皮递送包括对活性成分的穿过皮肤的至少一部分(但不一定所有的皮肤层)输送而不是仅局部施用于皮肤的外层的递送。
本公开整体涉及用于将包括微针阵列的微针装置施用于皮肤(或生物膜)以处理皮肤(即,在皮肤中产生小孔或穿孔或微孔)和/或将活性剂递送至皮肤的施用装置和方法。
参见图1-3,在一个实施方案中,施用装置100包括主体102,所述主体具有上部外壳104和下部外壳106,以及覆盖件108(在图2和3中移除)。上部外壳104可以能够由使用者容易抓握主体102的方式符合人体工程学地成形—使得其可贴合手部的手掌和/或施用装置100的重心可与用于抓握该施用装置100的手的中心对齐。上部外壳104包括外表面110和内表面112(参见,例如图14)。外表面110可包括粗糙表面修饰或其他表面修饰,以进一步使得使用者能够容易地抓握主体102。在实施方案中,出于美观目的和/或进一步使得使用者能够容易地抓握主体102,上部外壳104可在外表面110上包括橡胶抓握材料部分或其他医疗级材料。上部外壳104的内表面112可包括平滑表面修饰或其他表面修饰,诸如具有低表面能的表面修饰,以使得能够与下部外壳106的上部部分118的外表面124滑动接合,这将在下文进一步详细描述。在一个实施方案中,此类低表面能材料可优选地包括小于约37mj/mm2的表面能。在一个实施方案中,此类低表面能材料可优选地包括小于约29mj/mm2的表面能。在一个实施方案中,此类低表面能材料可优选地包括小于约18mj/mj/mm2的表面能。此类低表面能材料可包括聚乙酸乙烯酯(pva)、聚丙烯(pp)和聚四氟乙烯(ptfe)。在一个实施方案中,上部外壳104可包括顶盖113或其他结构,其可以为可移除的,因此使得能够进入和/或覆盖上部外壳104,以访问施用装置100的内部组件。在一个实施方案中,上部外壳104可由聚碳酸酯/丙烯腈丁二烯苯乙烯(pc/abs)制成,其可具有诸如低收缩、尺寸稳定性和结构刚度的特性。在其他实施方案中,上部外壳104可由具有高冲击强度的其他医疗级工程塑料制成。
覆盖件108被设计、构造和/或成形为覆盖、保护和/或包封下部外壳106并包封施用装置100的内部组件并且包括内表面(未示出)和外表面114。覆盖件108的内表面(未示出)可包括邻近覆盖件108的开口端(未示出)的一个或多个插片或突起部或其他结构(未示出),以与上部外壳104或主体102的其他部分上的唇缘115或其他结构配合,以有利于在施用装置100未被用于包封和/或保护施用装置100的内部组件时使覆盖件108保持在主体102上的适当位置。虽然当施用装置100未被使用时,此类结构防止覆盖件108从主体102脱落,但当此类使用者期望使用施用装置100时,使用者可手动移除覆盖件108。在一个实施方案中,施用装置100可包括防止覆盖件108被非预期或不允许的使用者使用或打开的结构,类似于用于“儿童防护”药物容器中的那些。覆盖件108还可包括一个或多个肋或凹槽116,如图所示,或能够容易地抓握覆盖件108的其他结构,但也可用作美观特征。在一个实施方案中,覆盖件108可由聚碳酸酯/丙烯腈丁二烯苯乙烯(pc/abs)制成,其可具有诸如低收缩、尺寸稳定性和结构刚度的特性。在其他实施方案中,覆盖件108可由具有高冲击强度的其他医疗级工程塑料制成。
参见图2和3,下部外壳106包括上部部分118、中部部分120和下部部分122。下部外壳106的上部部分118包括外表面124,所述外表面可具有平滑表面修饰或具有低表面能的其他修饰,以使得能够与上部外壳104的内表面112滑动接合。下部外壳106的上部部分118还可包括复位弹簧凹槽126和门弹簧凹槽128,下文将进一步详细地描述。下部外壳106的中部部分120(其可具有比下部外壳106的上部部分118和下部部分122更大的直径),可包括用于插入微针阵列载体140的狭槽130或开口,如下所述。在一个实施方案中,狭槽130可包括被示为凹口的一个或多个引导结构132,以用于将微针阵列载体140精确引导到适当位置,并确保微针阵列载体140不以不正确的取向诸如倒置插入狭槽130中。在另一个实施方案中,引导结构132可包括突出到狭槽130中的突起部,其与远离狭槽130延伸的凹口相对。狭槽130还可包括一个或多个肩部134,从而还使得能够将微针阵列载体140精确引导到适当位置并对应于微针阵列载体140的结构。下部外壳106的下部部分122可包括倒圆的或颈缩的部分136,所述部分可使下部部分122的下侧上的开口尺寸最小化,诸如大致对应于下文所述的待施用的微针阵列组件142的尺寸。下部部分122包括在其下侧上的下表面138。在一个实施方案中,下部外壳106或下部外壳106的特定部分可由聚碳酸酯/丙烯腈丁二烯苯乙烯(pc/abs)制成,其可具有诸如低收缩、尺寸稳定性和结构刚度的特性。在实施方案中,下部外壳106可由具有高冲击强度的其他医疗级工程塑料制成。在实施方案中,下部外壳106的下部部分122的内表面可包括具有有利的低表面能特性的聚丙烯(pp),其防止微针阵列组件142在施用期间粘着到下部外壳106。此类聚丙烯结构可在二次注模成型工艺中被模塑成刚性结构,其被构造为单独的组件,插入或安装到pc/abs部分中,或以其他方式与下部外壳106一起成形或成形为下部外壳。在另选的实施方案中,下部外壳106的下部部分122可具有与下部外壳106的上部部分118基本上相同的直径,以便在微针阵列组件142离开装置时为该微针阵列组件提供附加的内部间隙。
图4-9示出了微针阵列载体140。图4和5示出了不具有微针阵列组件142的微针阵列载体140并且图6-9示出了微针阵列载体140与设置在微针阵列载体140上的微针阵列组件142。微针阵列载体140包括顶侧144、底侧146、内表面148和外表面150。顶侧可包括一个或多个对齐的突起部152,其对应于主体102的下部外壳106上的狭槽130中所包括的引导结构132。在其中引导结构132形成为与凹口相对的突起部的实施方案中,对齐的突起部152可以为载体中与突起部或翅片相对的凹槽或凹口。对齐的突出部152可与微针阵列载体140基本上相同。在附加的实施方案中,对齐的突起部可短于微针阵列载体140的宽度。微针阵列载体140还可包括顶部表面144(如图所示)或底部表面146上的一个或多个固定插片154或突起部,以使得当微针阵列载体140定位在狭槽130中时,微针阵列载体140和狭槽130之间能够紧密贴合。
微针阵列载体140可包括柄部或抓握部分156,使得微针阵列载体140可容易地从任何包装中移除,承载并定位在施用装置100中,诸如进入狭槽130中。柄部156可包括结构,诸如肋状物158或其他表面特征或修饰,以增强抓握微针阵列载体140的容易性。抓握部分156还可包括倒圆边缘,以便在人体工程学上更有利于具有敏感手指的使用者。
微针阵列载体140可包括一个或多个插片或突起部160,诸如从内表面148延伸。如图6-9所示,微针阵列组件142可置于突起部160上。在该实施方案中,如下所述,微针阵列组件142可包括在基底166的下侧167上的粘合剂,诸如压敏粘合剂(psa),所述粘合剂与突起部160接触以将微针阵列组件142保持在突起部160上。在一个实施方案中,突起部160可被构造或尺寸设定成使得,在将微针阵列组件142保持在突起部160上时,在递送时,存在微针阵列组件142从突起部160移除的最小阻力,从而使得在由施用装置100施用期间能够有效地将微针阵列组件142递送到皮肤上。
微针阵列载体140可在由施用装置100施用期间通过提供刚性结构以提供对称的保持和释放力来适应微针阵列组件142到皮肤上的进一步有效递送,从而在微针阵列组件142从突起部160释放期间使突起部160的挠曲最小化。另外,可提供用于微针阵列载体140(具体地讲,用于突起部160)的低表面能材料,以适应微针阵列组件142在制造、包装期间和微针阵列组件142递送期间保持和释放。微针阵列载体140的外部结构可由具有有利特性(诸如低收缩、稳定尺寸和刚度)的工程塑料制成。微针阵列载体140的突起部160和内表面148可由聚丙烯制成,其可提供具有低表面能的有益效果,所述低表面能适应微针阵列组件142从突起部160释放,在药物涂覆期间拾取和放置,以及在施用期间将微针阵列组件142递送到皮肤。其他工程塑料也可用于微针阵列载体140。在一个实施方案中,此类低表面能材料可优选地包括小于约37mj/mm2的表面能。在一个实施方案中,此类低表面能材料可优选地包括小于约29mj/mm2的表面能。在一个实施方案中,此类低表面能材料可优选地包括小于约18mj/mj/mm2的表面能。此类低表面能材料可包括聚乙酸乙烯酯(pva)、聚丙烯(pp)和聚四氟乙烯(ptfe)。
参见图4-9,可包括微针阵列载体140中的间隙151并且其尺寸可被设计成大于柱塞柱子194的宽度195或直径。如下所述,这可使得阵列载体140能够在柱塞174已被击发之后移除,这可使得使用者能够在使用之间以未装填状态或构型储存施用装置100。在一个实施方案中,微针阵列载体140通常呈环的形状,其具有呈环形的间隙151。微针阵列组件140可定位在环或边界的内表面之间。在实施方案中,间隙151大于柱塞柱子194的宽度或直径。在实施方案中,间隙151最初略小于柱塞柱子194的宽度或直径,但由柔性材料构成,使得间隙151可被挠曲成大于柱塞柱子194的宽度或直径。
参见图10-13,其示出了微针阵列组件142,其在本文中也可称为“微针装置”或“贴片”,并且可包括微针164的阵列162(或统称为“微针阵列”)和任何支撑结构或基底166,其用于支撑微针阵列162和/或将微针阵列162联接到施用装置100的其他结构或组件,诸如突起部160。
如上所述,在一些实施方案中,活性成分或活性剂(例如,药物)可经由微针164(例如,经由实心微针或空心微针,如下所述)递送。可掺入到本公开的施用装置中的药物活性剂(也被称为“药物”)的示例为能够在施用于皮肤时局部作用或全身作用的那些。一些示例包括可以透皮装置形式商购获得的丁丙诺啡、可乐定、双氯芬酸、雌二醇、格拉司琼、硝酸异山梨酯、左炔诺孕酮、利多卡因、哌甲酯、烟碱、硝酸甘油、奥昔布宁、利凡斯的明、罗替戈汀、东莨菪碱、司来吉兰、睾酮、妥洛特罗、和芬太尼。其他示例包括甾族(如,氢化可的松、泼尼松龙、曲安西龙)和非甾族(如,萘普生、吡罗昔康)两者的抗炎剂药物;抑菌剂(如,氯已定、己基间苯二酚);抗菌剂(例如,诸如青霉素v的青霉素、诸如头孢氨苄的先锋霉素、红霉素、四环素、庆大霉素、磺胺噻唑、硝基呋喃妥因、以及诸如诺氟沙星、氟甲喹、和依巴沙星的喹诺酮);抗原生动物药(例如,甲硝唑);杀真菌剂(例如,制霉菌素);冠状血管扩张药;钙通道阻滞剂(例如,硝苯啶、硫氮卓酮);支气管扩张剂(例如,茶碱、吡布特罗、沙美特罗、异丙去甲肾上腺素);酶抑制剂,诸如,胶原酶抑制剂、蛋白酶抑制剂、乙酰胆碱酯酶抑制剂(例如,多奈哌齐)、弹性蛋白酶抑制剂、脂氧合酶抑制剂(例如,a64077)、和血管紧张素转化酶抑制剂(例如,卡托普利、赖诺普利);其他抗高血压药(例如,普萘洛尔);白三烯拮抗剂(如,ici204,219);抗溃疡剂,诸如h2拮抗剂;甾族激素(例如,孕酮);抗病毒药和/或免疫调节剂(例如,1-异丁基-1h-咪唑并[4,5-c]喹啉基-4-胺、1-(2-羟基-2-甲基丙基)-1h-咪唑并[4,5-c]喹啉基-4-胺、n-[4-(4-氨基-2-乙基-1h-咪唑并[4,5-c]喹啉基-1-基)丁基]甲烷磺酚胺、和阿昔洛韦);局部麻醉剂(例如,苯佐卡因、异丙酚、丁卡因、丙胺卡因);强心剂(例如,洋地黄、地高辛);镇咳药(例如,可待因、右美沙芬);抗组胺剂(例如,苯海拉明、扑尔敏、特非那定);麻醉性止痛药(例如,吗啡、枸橼酸芬太尼、舒芬太尼、盐酸氢吗啡酮);肽激素(例如,人或动物生长激素、lhrh、甲状旁腺激素);强心产品,诸如心房肽;抗糖尿病剂(例如,胰岛素、艾塞那肽);酶(例如,抗牙斑酶、溶菌酶、葡聚糖酶);抗呕吐剂;抗惊厥剂(例如,乙胺嗪);免疫抑制剂(例如,环孢菌素);精神治疗剂(例如,安定);镇静剂(例如,镇静安眠剂);抗凝血药(例如,肝素、依诺肝素钠);止痛药(例如,对乙酰氨基酚);抗偏头痛药剂(例如,麦角胺、褪黑激素、舒马曲坦、佐米曲坦);抗心律失常剂(例如,氟卡尼);止吐药(例如,胃复安、昂丹司琼、盐酸格拉司琼);抗癌剂(例如,氨甲蝶呤);神经剂,诸如抗焦虑药;止血剂;抗肥胖剂;多巴胺激动剂(例如,阿扑吗啡);gnrh激动剂(例如,亮丙瑞林、戈舍瑞林、那法瑞林);生育激素(例如,hcg、hmg、尿促卵泡素);干扰素(例如,干扰素-α、干扰素-β、干扰素-γ、聚乙二醇化干扰素-α);等等,以及其药学上可接受的盐和酯。构成治疗有效剂量的药量可由本领域技术人员适当考虑特定药物、特定载体和所期望的治疗效果来轻易地确定。
在一些实施方案中,肽治疗剂(天然的、合成的或重组的)可经由微针164(例如,经由实心微针或空心微针,如下所述)递送。可掺入到本公开的施用装置中的肽治疗剂的示例包括甲状旁腺激素(pth)、甲状旁腺激素相关蛋白(pthrp)、降钙素、溶菌酶、胰岛素、促胰岛素类似物、醋酸格拉默、醋酸戈舍瑞林、生长抑素、奥曲肽、亮丙瑞林、加压素、去氨加压素、胸腺素α-1、心房利钠肽(anp)、内啡肽、血管内皮生长因子(vegf)、成纤维细胞生长因子(fgf)、促红细胞生成素(epo)、骨形态发生蛋白(bmp)、表皮生长因子(efg)、粒细胞集落刺激因子(g-csf)、粒巨噬细胞集落刺激因子(gm-csf)、类胰岛素生长因子(igf)、血小板衍生生长因子(pdgf)、生长激素释放激素(ghrh)、阿法链道酶、组织纤溶酶原激活剂(tpa)、尿激酶、anp清除酶抑制剂、黄体生成激素释放激素(lhrh)、黑素细胞刺激激素(α和βmsh)、垂体激素(hgh)、促肾上腺皮质激素(acth)、人绒毛膜促性腺激素(hcg)、链激酶、白细胞介素(例如,il-2、il-4、il-10、il-12、il-15、il-18)、蛋白c、蛋白s、血管紧张素、血管生成素、内皮素、喷替吉肽、脑利钠肽(bnp)、神经肽y、胰岛淀粉样多肽(iapp)、血管活性肠肽(vip)、水蛭素、胰高血糖素、催产素、以及前述肽治疗剂中任一种的衍生物。
在一些实施方案中,具有大分子量的药物可在鼻内递送。增加药物的分子量通常可引起无助透皮递送的减少。此类大分子的示例包括蛋白、肽、核苷酸序列、单克隆抗体、疫苗、多糖(诸如,肝素)、和抗生素(诸如,头孢曲松)。合适疫苗的示例包括治疗性癌症疫苗、炭疽疫苗、流感疫苗、莱姆病疫苗、狂犬病疫苗、麻疹疫苗、腮腺炎疫苗、水痘疫苗、天花疫苗、肝炎疫苗、甲肝疫苗、乙肝疫苗、丙肝疫苗、百日咳疫苗、风疹疫苗、白喉疫苗、脑炎疫苗、乙脑疫苗、呼吸道合胞病毒疫苗、黄热病疫苗、重组蛋白疫苗、dna疫苗、脊髓灰质炎疫苗、治疗性癌症疫苗、疱疹疫苗、人类乳头状瘤病毒疫苗、肺炎球菌疫苗、流脑疫苗、百日咳疫苗、破伤风疫苗、伤寒疫苗、霍乱疫苗、结核病疫苗、严重急性呼吸道症候群(sars)疫苗、hsv-1疫苗、hsv-2疫苗、艾滋病疫苗以及它们的组合。术语“疫苗”因此包括但不限于呈蛋白质、多糖、寡糖、或减弱或杀死病毒的形式的抗原。适宜的疫苗和疫苗佐剂的附加示例描述于美国专利申请公布2004/0049150(dalton等人)中,其公开内容全文以引用方式并入本文。
在另一个实施方案中,可使用原本难以或不可能通过被动透皮递送来递送的小分子药物。这些分子的示例包括:盐型;离子型分子,诸如二膦酸盐,包括阿仑膦酸钠或帕米膦酸钠(sodiumpamedronate);和具有无利于被动透皮递送的物理化学特性的分子。
可用于实施本公开的微针阵列162可具有诸如以下专利和专利申请中所述的各种构造和特征,这些专利或专利申请的公开内容全文以引用方式并入本文。微针阵列162的一个实施方案包括在以下专利中公开的结构:美国专利申请公布2005/0261631(clarke等人),其描述了具有截顶锥形形状和受控纵横比的微针。微针阵列的另一个实施方案包括在以下专利中公开的结构:美国专利6,091,975(daddona等人),其描述了用于刺穿皮肤的刀片状微突起。微针阵列的另一个实施方案包括在以下专利中公开的结构:美国专利6,312,612(sherman等人),其描述了具有空心中央通道的锥形结构。微针阵列的另一个实施方案包括在以下专利中公开的结构:美国专利6,379,324(gartstein等人),其描述了在微针的尖端的顶表面处具有至少一个纵向刀片的空心微针。微针阵列的另一个实施方案包括在以下专利中公开的结构:美国专利申请公布us2012/0123387(gonzalez等人)和us2011/0213335(burton等人),这两者描述了空心微针。微针阵列的另一个实施方案包括在以下专利中公开的结构:美国专利6,558,361(yeshurun)和7,648,484(yeshurun等人),这两者描述了空心微针阵列及其制造方法。
可用于本公开的微针阵列中的微针的各种实施方案描述于pct公布wo2012/074576(duan等人)中,其描述了液晶聚合物(lcp)微针;以及pct公布wo2012/122162(zhang等人)中,其描述了可用于本公开的微针的多种不同类型和组成的微针。
在一些实施方案中,微针材料可为(或包括)有机硅、玻璃、或金属诸如不锈钢、钛、或镍钛合金。在一些实施方案中,微针材料可为(或包括)聚合物材料,优选地医疗级聚合物材料。示例性类型的医疗级聚合物材料包括聚碳酸酯、液晶聚合物(lcp)、聚醚醚酮(peek)、环烯烃共聚物(coc)、聚对苯二甲酸丁二醇酯(pbt)。优选类型的医疗级聚合物材料包括聚碳酸酯和lcp。
在一些实施方案中,微针材料可为(或包括)可生物降解的聚合物材料,优选地医疗级可生物降解的聚合物材料。示例性类型的医疗级可生物降解的材料包括聚乳酸(pla)、聚乙醇酸(pga)、pga和pla共聚物、聚酯-酰胺聚合物(pea)。
在一些实施方案中,微针可由可溶解、可降解或可崩解的材料制备,在本文被称为“可溶解微针”。可溶解、可降解或可崩解的材料为在使用期间溶解、降解或崩解的任何固体材料。具体地讲,“可溶解微针”在角质层下面的组织中充分溶解、降解或崩解,以允许治疗剂释放到组织中。治疗剂可涂布在可溶解微针上或掺入可溶解微针中。在一些实施方案中,可溶解材料选自碳水化合物或糖。在一些实施方案中,可溶解材料为聚乙烯吡咯烷酮(pvp)。在一些实施方案中,可溶解材料选自由:透明质酸、羧甲基纤维素、羟丙基甲基纤维素、甲基纤维素、聚乙烯醇、蔗糖、葡萄糖、葡聚糖、海藻糖、麦芽糖糊精、以及它们的组合。
在一些实施方案中,微针可由任何上述材料中的两种或更多种材料的组合制成(或包括任何上述材料中的两种或更多种材料的组合)。例如,微针的尖端可为可溶解材料,而微针的其余部分为医疗级聚合物材料。
可用于实施本公开的微针阵列中的单根微针或多根微针可具有能够刺穿角质层的各种形状。在一些实施方案中,多根微针中的一根或多根可具有四方锥体形状、三角锥体形状、阶梯锥体形状、圆锥形状、微刀片形状、或皮下注射针的形状。在一些实施方案中,多根微针中的一根或多根可具有四方锥体形状。在一些实施方案中,多根微针中的一根或多根可具有三角锥体形状。在一些实施方案中,多根微针中的一根或多根可具有阶梯锥体形状。在一些实施方案中,多根微针中的一根或多根可具有圆锥形状。在一些实施方案中,多根微针中的一根或多根可具有微刀片形状。在一些实施方案中,多根微针中的一根或多根可具有皮下注射针的形状。所述形状可为对称的或非对称的。所述形状可为截顶的(例如,多根微针可具有截棱锥形状或截头原锥形状)。在优选实施方案中,微针阵列中的多根微针各自具有四方锥体形状。
在一些实施方案中,微针阵列中的多根微针为实心微针(即,所述微针为通体实心的)。在一些实施方案中,实心微针阵列中的多根实心微针可具有四方锥体形状、三角锥体形状、阶梯锥体形状、圆锥形状或微刀片形状。在优选的实施方案中,实心微针阵列中的多根实心微针各自具有四方锥体形状。
在一些实施方案中,微针阵列中的多根微针为空心微针(即,所述微针包含贯通微针的空心膛孔)。空心膛孔可从微针的基部到微针的尖端或膛孔可从微针的基部到与微针的尖端错开的位置。在一些实施方案中,空心微针阵列中的多根空心微针中的一根或多根可具有圆锥形状、圆柱形状、四方锥体形状、三角锥体形状、或皮下注射针的形状。
在一些实施方案中,空心微针阵列中的多根空心微针中的一根或多根可具有圆锥形状。在一些实施方案中,空心微针阵列中的多根空心微针中的一根或多根可具有圆柱形状。在一些实施方案中,空心微针阵列中的多根空心微针中的一根或多根可具有四方锥体形状。在一些实施方案中,空心微针阵列中的多根空心微针中的一根或多根可具有三角锥体形状。在一些实施方案中,空心微针阵列中的多根空心微针中的一根或多根可具有皮下注射针的形状。在优选的实施方案中,空心微针阵列中的多根空心微针各自具有常规皮下注射针的形状。
图13示出了包括定位在基底166上的四根微针164的微针阵列162的一部分。每根微针164具有高度h,该高度h为从微针164的尖端到基底166处微针164基部的长度。单根微针164的高度或微针阵列162上的所有微针164的平均高度可称为微针的高度h。在一些实施方案中,多根微针164中的每一根(或所有多根微针164的平均值)具有约100微米至约3000微米,在一些实施方案中约100微米至约1500微米,在一些实施方案中约100微米至约1200微米,且在一些实施方案中约100微米至约1000微米的高度。
在一些实施方案中,多根微针164中的每一根(或所有多根微针164的平均值)具有约200微米至约1200微米、约200微米至约1000微米、约200微米至约750微米、或约200微米至约600微米的高度。
在一些实施方案中,多根微针中的每一根(或所有多根微针的平均值)具有约250微米至约1500微米、约500微米至约1000微米、或约500微米至约750微米的高度。
在一些实施方案中,多根微针164中的每一根(或所有多根微针164的平均值)具有约800微米至约1400微米的高度。
在一些实施方案中,多根微针164中的每一根(或所有多根微针164的平均值)具有约500微米的高度。
在一些实施方案中,多根微针164中的每一根(或所有多根微针164的平均值)具有小于约3000微米的高度。在其他实施方案中,多根微针164中的每一根(或所有多根微针164的平均值)具有小于约1500微米的高度。在另一些其他实施方案中,多根微针164中的每一根(或所有多根微针164的平均值)具有小于约1200微米的高度。在另一些其他实施方案中,多根微针164中的每一根(或所有多根微针164的平均值)具有小于约1000微米的高度。在另一些实施方案中,多根微针164中的每一根(或所有多根微针164的平均值)具有小于约750微米的高度。在另一些其他实施方案中,多根微针164中的每一根(或所有多根微针164的平均值)具有小于约600微米的高度。
在一些实施方案中,多根微针164中的每一根(或所有多根微针164的平均值)具有至少约100微米的高度。在其他实施方案中,多根微针164中的每一根(或所有多根微针164的平均值)具有至少约200微米的高度。在另一些其它实施方案中,多根微针164中的每一根(或所有多根微针164的平均值)具有至少约250微米的高度。在另一些实施方案中,多根微针164中的每一根(或所有多根微针164的平均值)具有至少约500微米的高度。在另一些其它实施方案中,多根微针164中的每一根(或所有多根微针164的平均值)具有至少约800微米的高度。
在采用实心微针164的一些实施方案中,多根实心微针164中的每一根(或所有多根实心微针的平均值)具有约100微米至约1500微米、约100微米至约1200微米、约200微米至约1000微米、约200微米至约750微米、约200微米至约600微米、或约500微米的高度。
在采用空心微针的一些实施方案中,多根空心微针中的每一根(或所有多根空心微针的平均值)具有约100微米至约3000微米、约800微米至约1400微米、或约500微米的高度。
在一些实施方案中,多根空心微针中的每一根(或所有多根空心微针的平均值)具有约900至约1000微米的高度。在其他实施方案中,多根空心微针中的每一根(或所有多根空心微针的平均值)具有约900至约950微米的高度。在另一些其他实施方案中,多根空心微针中的每一根(或所有多根空心微针的平均值)具有约900微米的高度。
微针阵列中的单根微针或多根微针164也可由其纵横比表征。微针的纵横比为微针的高度h相对宽度(在微针的基部处)w的比率(如图7所示)。纵横比可以表示为h:w。在一些实施方案中,多根微针164中的每一根(或所有多根微针164的平均值)具有在2:1至5:1的范围内的纵横比。在一些这样的实施方案中,多根微针164中的每一根(或所有多根微针164的平均值)具有至少3:1的纵横比。
在一些实施方案中,微针阵列164包含每平方厘米微针阵列约100根至约1500根微针。
在采用实心微针的一些实施方案中,实心微针阵列包含每平方厘米实心微针阵列约100至约1500根实心微针。
在一些实施方案中,实心微针阵列包含每平方厘米实心微针阵列约200至约500根实心微针。
在一些实施方案中,实心微针阵列包含每平方厘米实心微针阵列约300根至约400根实心微针。
在采用空心微针的一些实施方案中,空心微针阵列包含每空心微针阵列约3至约30根空心微针。
在一些实施方案中,空心微针阵列包含每空心微针阵列约10至约30根空心微针。
在一些实施方案中,空心微针阵列包含每空心微针阵列约3根至约20根空心微针。
在一些实施方案中,空心微针阵列包含每空心微针阵列约13根至约20根空心微针。
在一些实施方案中,空心微针阵列包含每空心微针阵列约8根至约18根空心微针。
在一些实施方案中,空心微针阵列包含每空心微针阵列约18根空心微针。
在一些实施方案中,空心微针阵列包含每空心微针阵列约12根空心微针。
在一些实施方案中,微针阵列中的多根微针中的每一根(或所有多根微针的平均值)可穿透到皮肤中达约50微米至约1500微米、约50微米至约400微米、或约50微米至约250微米的深度。
在一些实施方案中,微针阵列中的多根微针中的每一根(或所有多根微针的平均值)可穿透到皮肤中达约100至约400微米、或约100至约300微米的深度。
在一些实施方案中,微针阵列中的多根微针中的每一根(或所有多根微针的平均值)可穿透到皮肤中达约150微米至约1500微米、或约800微米至约1500微米的深度。
在一些实施方案中,微针阵列中的多根微针中的每根微针(或所有多根微针的平均值)可穿透到皮肤中达约400微米至约800微米的深度。
对于所有上述实施方案,将了解,微针阵列中的多根微针中的每根微针的穿透深度(dop)(或所有多根微针的平均值)可能不是微针本身的全长。
在一些实施方案中,根据本公开的微针阵列组件142可以呈贴片的形式。此类实施方案的一个示例在图10-12中更详细地示出。微针阵列组件142包括微针阵列162,存在于基底166上的压敏粘合剂。微针阵列162示出为具有从微针基底166伸出的微针164。微针164可以任何期望的图案布置或者无规地分布在基底166上。如图所示,微针164以均匀间隔的行布置。当以行布置时,可将行布置成使得微针164对齐或偏移。在一些实施方案(未示出)中,微针164可以多边形图案布置,诸如三角形、四方形、矩形、五边形、六边形、七边形、八边形或梯形。在其他实施方案(未示出)中,微针164可以圆形或椭圆形图案布置。
在一些实施方案中,由微针覆盖的基底的表面积为约0.1cm2至约20cm2。在一些这样的实施方案中,由微针覆盖的基底的表面积为约0.5cm2至约5cm2。在一些其他这样的实施方案中,由微针覆盖的基底的表面积为约1cm2至约3cm2。在另一些其他这样的实施方案中,由微针覆盖的基底的表面积为约1cm2至约2cm2。
在一些实施方案中,本公开的微针可设置在阵列的基本上整个表面上。在其他实施方案(未示出)中,基底的一部分可不设置有微针(即,基底的一部分为非结构化的)。在一些这样的实施方案中,非结构化表面具有大于面向皮肤表面的装置表面的总面积的约1%且小于约75%的面积。在这些实施方案中的另一个实施方案中,非结构化表面具有大于约0.65cm2(0.10平方英寸)至小于约6.5cm2(1平方英寸)的面积。
对于空心微针,空心通道或膛孔延伸穿过基底和微针。在一些实施方案中,膛孔在空心微针的尖端处或附近的通道开口处退出。通道优选地在空心微针的尖端附近的开口处退出。最优选地,通道或膛孔沿着微针的中心轴线继续,但类似于皮下注射针在微针的倾斜侧壁上退出,以有助于防止在插入时组织堵塞通道。在一些实施方案中,通道膛孔的直径为约10微米至约200微米。在其他实施方案中,通道镗孔的直径为约10至约150微米。在另一些其他实施方案中,通道镗孔的直径为约30至约60微米。
在空心微针的一些实施方案中,通道膛孔的平均截面积为约75至约32,000微米。在空心微针的其他实施方案中,通道膛孔的平均截面积为约75至约18,000微米。在空心微针的另一些其他实施方案中,通道膛孔的平均截面积为约700至约3,000微米。
在空心微针阵列的一些实施方案中,邻近微针之间的平均间距(如从微针尖端到微针尖端测量)在约0.7mm与约20mm之间。在空心微针阵列的其他实施方案中,邻近微针之间的平均间距在约0.7mm与约10mm之间。在空心微针阵列的另一些其他实施方案中,邻近微针之间的平均间距在约2mm与约20mm之间。在空心微针阵列的另一些其他实施方案中,邻近微针之间的平均间距在约2mm与约10mm之间。在空心微针阵列的优选的实施方案中,邻近微针之间的平均间距在约2mm之间。
在空心微针阵列的一些实施方案中,邻近微针之间的平均间距(如从微针尖端到微针尖端测量)大于约0.7mm。在空心微针阵列的其他实施方案中,邻近微针之间的平均间距大于约2mm。
在空心微针阵列的一些实施方案中,邻近微针之间的平均间距小于约20mm。在空心微针阵列的其他实施方案中,邻近微针之间的平均间距小于约10mm。
在实心微针阵列的一些实施方案中,邻近微针之间的平均间距(如从微针尖端到微针尖端测量)在约200微米与约2000微米之间。在实心微针阵列的其他实施方案中,邻近微针之间的平均间距在约200微米与约600微米之间。在实心微针阵列的另一些其他实施方案中,邻近微针之间的平均间距在约200微米与约300微米之间。在实心微针阵列的另一些其他实施方案中,邻近微针之间的平均间距在约500微米与约600微米之间。
在实心微针阵列的一些实施方案中,邻近微针之间的平均间距(如从微针尖端到微针尖端测量)大于约200微米。在实心微针阵列的其他实施方案中,邻近微针之间的平均间距大于约500微米。
在实心微针阵列的一些实施方案中,邻近微针之间的平均间距小于约2000微米。在实心微针阵列的其他实施方案中,邻近微针之间的平均间距小于约1000微米。在实心微针阵列的另一些其他实施方案中,邻近微针之间的平均间距小于约600微米。在实心微针阵列的另一些其他实施方案中,邻近微针之间的平均间距小于约300微米。
所述微针阵列可以任何合适的方式制成,诸如通过注射模制、压缩模制、金属注射模制、压印、光蚀刻或挤出而制成。在一个实施方案中,空心微针阵列可通过下述方式而制成:注射模制聚合物(诸如医疗级聚碳酸酯或lcp),之后进行激光钻孔,以形成微针的通道。
参见图14-20,在实施方案中,施用装置100包括闩锁168、套筒170、门172、柱塞174、以及各种弹簧或其他偏置构件。闩锁168的形状可以为大致圆柱形,并且可包括上凸缘部分176,所述上凸缘部分具有从上凸缘部分176延伸的一个或多个插片178。闩锁168可包括限定在闩锁168的外表面182中的凹槽180。闩锁168可包括围绕其轴线限定的闩锁孔184或开孔,其中具有扣件185(参见图21-26),该轴线与施用装置100的轴线x同轴(图14)。
套筒170的形状可以为大致圆柱形,并且包括顶侧186上的闩锁凹槽186和围绕其轴线限定的套筒孔188或开孔,该轴线与施用装置100的轴线x同轴(图14)。套筒还可包括限定在其下侧上的击发弹簧凹槽190。
门172的形状可以为大致圆柱形,并且可包括靠近其下端的一个或多个插片192或闩锁。在实施方案中,门172可以为期望的颜色或包括其下端上的标记,使得使用者可容易地观察门172在操作中是打开的还是闭合的,如下所述。
柱塞174可包括具有宽度195或直径的柱塞柱子194,所述柱子194可包括一个或多个翅片196(在一个实施方案中,诸如图14-24所示的)、第一柱塞盘198和邻近其下端的第二柱塞盘200。柱塞可包括邻近其上端204的插片202或闩锁。在一个实施方案中,诸如图27和28所示,柱塞柱子194不包括翅片196,而是大致圆柱形形状并且包括两个凸轮插片202,这在下文进一步描述。
施用装置100的弹簧可包括闩锁弹簧206,其邻近闩锁168设置,诸如示于闩锁168下方,并且与闩锁168和套筒170配合;复位弹簧208,其邻近上部外壳104和下部外壳106设置并定位在限定在下部外壳106中的复位弹簧凹槽126中;插入或击发弹簧210,其邻近套筒170和存在于柱塞174上的第一柱塞盘198设置,定位在限定于套筒170中的击发弹簧凹槽190中;以及门弹簧212,其邻近下部外壳106和门172设置并定位在限定在下部外壳106中的门弹簧凹槽128中。在实施方案中,除了压缩弹簧之外的偏置构件(诸如板簧、橡胶构件或结构)可用于代替压缩弹簧或作为压缩弹簧的替代物。
在实施方案中,闩锁168、套筒170和柱塞174可由聚甲醛(pom)工程热塑性塑料制成。此类pom可包括得自杜邦公司(duponttm)的
在实施方案中,闩锁弹簧206、复位弹簧208、击发弹簧210和门弹簧212可由不锈钢类型302制成。在其他实施方案中,闩锁弹簧206、复位弹簧208、击发弹簧210和门弹簧212可由适用于医疗装置的其他材料制成。
在实施方案中,门172由包括高冲击强度的材料制成,诸如pc/abs,诸如sabic
参见图14,在使用中,下部外壳106的下部部分122的下表面138被放置成与皮肤或另一表面(诸如无菌或卫生表面“s”)接触。上部外壳104沿施用装置100的轴线x轴向向下推动,使得上部外壳104的内表面112在下部外壳106的外表面124上方滑动并且击发弹簧210被压缩,并因此被供能。该被供能的击发弹簧210稍后用于从施用装置100驱动微针阵列组件142。
参见图15,当上部外壳104沿施用装置100的轴线x轴向向下推动时,击发弹簧210被压缩并因此被供能。当发生这种情况时,复位弹簧208也被压缩。另外,当上部外壳104沿施用装置100的轴线x轴向向下推动时,闩锁168由于闩锁168与柱塞柱子194的上端的相互作用而围绕轴线x旋转地移位。具体地讲,参见图21-26,示出了闩锁168和柱塞174在施用装置100的未装填状态和装填状态之间的相互作用。当上部外壳104轴向向下推动时,闩锁168在顺时针方向上围绕轴线x旋转地移位,这是由于闩锁168上的倾斜表面187与柱塞174上的倾斜表面203的相互作用。随着柱塞174继续轴向向上移动到闩锁168的膛孔184中,闩锁168继续在顺时针方向上旋转直至闩锁168的倾斜表面187能够滑过插片202的倾斜表面203,使得由闩锁弹簧206产生的闩锁168的逆时针扭转力导致闩锁168以逆时针方式向后旋转,直至柱塞174的上端204上的插片202可接合闩锁孔184中的扣件185并与该扣件联接。图25示出了在装填之前的施用装置的顶部平面图(其中顶盖113被移除),其中插片202尚未与扣件185接合。图26示出了装填之后的施用装置的顶部平面图(其中顶盖113被移除),其中插片202已与扣件185接合。
在装填施用装置100后,如果使用者从上部外壳104释放压缩压力,则施用装置100返回至伸长位置,如图16所示,这是由于复位弹簧208返回到未压缩状态。由于插片202和扣件185可操作地互锁并且柱塞174向上拉伸到上部外壳104中,所以插入或击发弹簧210保持压缩或供能。因为门172的插片192与柱塞174的第二柱塞盘200接合并联接,所以当柱塞174向上拉伸时,其带动门172与其一起向上拉伸。参见图14和15,其中能够插入微针阵列载体140的狭槽130最初在门172的底端处被门172覆盖。当施用装置100处于图16所示的位置时,向上拉伸门172(和底端),从而打开狭槽130。这使得当施用装置100已被装填并且准备使用时,微针阵列载体140仅能够被插入狭槽130中。这也允许患者通过观察窗是打开的还是闭合的来容易地观察施用装置100是否已被装填或未装填。参见图17和18,一旦从狭槽130移除门172的下端,微针阵列载体140就能够插入狭槽130中。
参见图17,一旦具有微针阵列组件142的微针阵列载体140已插入狭槽130中,微针阵列组件142就可通过在上部外壳104上再次轴向压缩(即,向下推动)而施用于皮肤。这使得闩锁168以顺时针方式旋转,这通过释放柱塞174的上端204处的插片202来释放弹簧加载的柱塞174—插片202和扣件185彼此可操作地滑动,直至不再接合并且击发弹簧210释放到其未压缩状态。弹簧加载的柱塞174的第二柱塞盘200可被定位成一旦被装填就直接抵靠或非常靠近微针阵列组件142的下侧167,或当上部外壳104再次轴向向下按压但在柱塞174释放之前(即,施用装置100击发之前)非常接近微针阵列组件142的底部表面167进行直接接触。通过具有这种构型,使用者可防止当柱塞加速并撞击微针阵列组件以便在仍处于施用装置中时将其从载体中释放出来时可能出现的不稳定问题。相反,当柱塞开始加速并在与微针阵列组件142接触皮肤的大约同时或基本上同时到达期望的冲击速度时,柱塞174将微针阵列组件142从微针阵列载体140推出。
图27和28示出了在已将微针阵列组件142施用于表面之后,根据一个实施方案的柱塞174的闩锁的扣件185和插片202,其中如上所述,柱塞174和其上的插片202的形状包括与图1-24中所示的形状不同的形状。本领域的技术人员将认识到,可使用柱塞174和插片202的另外的形状和构型。
参见图20,在一个实施方案中,微针阵列组件142不固定或保持在柱塞174的第二柱塞盘200上,因此一旦将其施用于患者的皮肤,就不需要使施用装置100(即,柱塞174的第二柱塞盘200)与微针阵列组件142分离。微针阵列组件142附连到皮肤,并且可在不干扰微针阵列组件142的情况下移除施用装置100。
在已递送微针阵列组件142并将其附连到患者之后,微针阵列载体140可从狭槽130移除,从而使施用装置返回至其初始取向。由于其形状,例如其“c”形,尽管柱塞174(包括柱塞柱子194)处于其伸长位置,但通常与柄部156相对的微针阵列载体140上的开口端使得微针阵列载体140能够从施用装置100中的狭槽130移除。
本文引用的专利、专利文献和出版物的全部公开内容均全文以引用方式并入本文,如同每个文件都单独并入一样。在不脱离本发明的范围和实质的前提下,本发明的各种变型和更改对本领域的技术人员而言将显而易见。应当理解,本发明并非意图不当地限制于本文所示出的示例性实施方案和实施例,并且上述实施例和实施方案仅以举例的方式提出,而且本发明的范围旨在仅受下面本文所示出的权利要求书的限制。
- 还没有人留言评论。精彩留言会获得点赞!